Mukopolysacharidózy z pohledu otorinolaryngologa
ENT Manifestation of Mucopolysaccharidoses
The mucopolysaccharidoses belong to the large group of inherited metabolic disorders. The primary pathophysiologic basis lies in a deficiency of specific lysosomal hydrolytic enzymes leading to an accumulation of glycosaminoglycans (originally mucopolysaccharides) in the lysosomes and extracellular tissues. Multisystemic and highly variable clinical manifestations include craniofacial dysmorphy, musculoskeletal involvement, joint contractures, hepato-and splenomegaly, inguinal or umbilical hernias and eventually cognitive impairment. Ear, nose, and throat problems are very common and are often among the first symptoms to appear already in the early childhood. ENT manifestation invariably includes otological involvement (recurrent acute otitis media, otitis media with effusion, hearing loss), adenotonsillar hypertrophy and progressive airway obstruction. Thus, otorhinolaryngologist has an integral role in early recognition of the disease, in initiating of further examination leading to the diagnosis of MPS and future management and treatment of children with mucopolysaccharidoses.
Keywords:
mucopolysaccharidoses, recurrent acute otitis media, hearing disorder
Authors:
Lenka Murgašová
; M. Jurovčík; V. Biskupová; J. Pavlíčková; M. Magner
Authors‘ workplace:
Klinika dětského a dorostového lékařství 1. LF UK a VFN, Praha
Published in:
Otorinolaryngol Foniatr, 67, 2018, No. 3, pp. 62-67.
Category:
Review Article
Overview
Mukopolysacharidózy patří mezi dědičné metabolické poruchy. Primárním patofyziologickým principem je deficit některého z lysosomálních hydrolytických enzymů vedoucích ke střádání glykosaminoglykanů (dříve mukopolysacharidů) v lysosomech a extracelulární tkáni. Postižení je multisystémové s širokou klinickou variabilitou a zahrnuje dysmorfické rysy obličeje, postižení skeletu, kloubní kontraktury, hepato - a splenomegalii, tříselnou či pupeční kýlu, případně mentální postižení. Příznaky v ORL oblasti jsou velice časté a mnohdy se jedná o první manifestaci onemocnění již v batolecím věku. Jde především o otologickou problematiku (recidivující akutní otitida, sekretorická otitida, porucha sluchu), adenotonzilární hypertrofii a progresivní obstrukci dýchacích cest. Otorinolaryngolog tak hraje důležitou roli v rozpoznání nemoci, v iniciaci dalšího vyšetření vedoucího k diagnostice onemocnění a umožnění časného zahájení léčby.
Klíčová slova:
mukopolysacharidózy, recidivující akutní otitida, porucha sluchu
1. ÚVOD
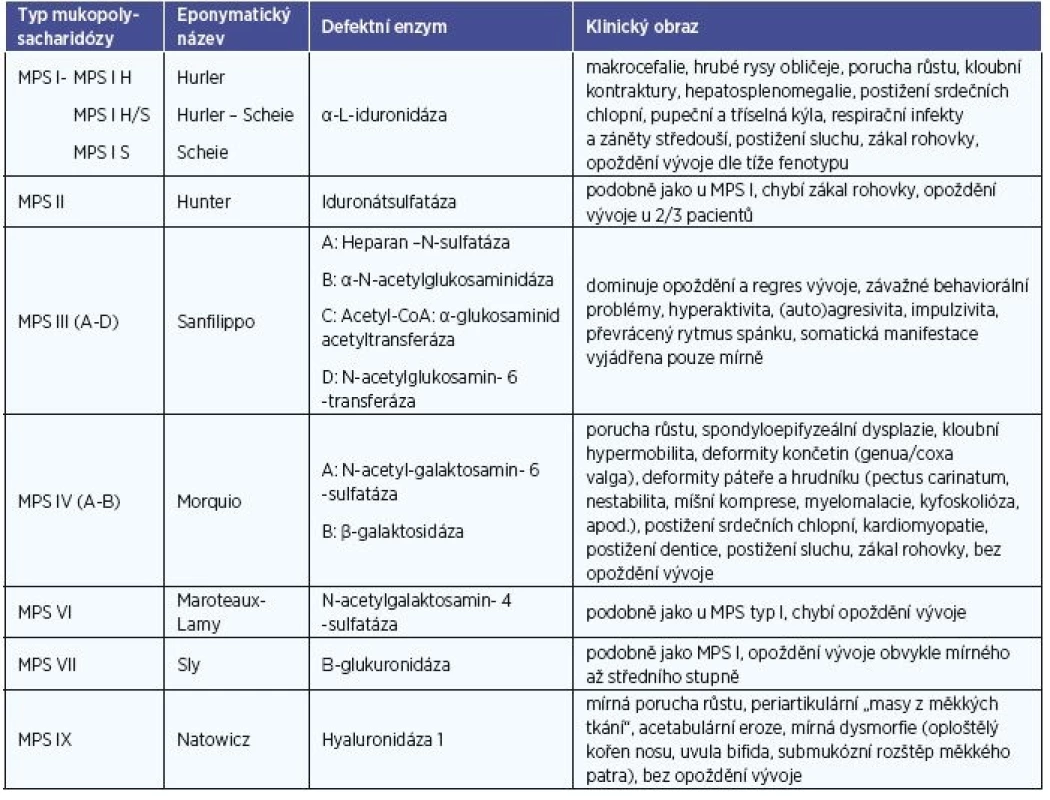
Mukopolysacharidózy (MPS) patří do skupiny více než šedesáti známých geneticky podmíněných lysosomálních střádavých onemocnění (tab. 1) (18). Jejich příčinou je nedostatečná aktivita některého z lysosomálních enzymů podílejících se na degradaci glykosaminoglykanů (GAG), dříve nazývaných mukopolysacharidy. Parciálně degradované GAG se střádají v lysosomech a extracelulární matrix řady tkání (17). Významnou roli hrají indukované sekundární patofyziologické kaskády. Tyto zahrnují aberantní genovou expresi, indukci prozánětlivého stavu a oxidačního stresu, aberantní fagocytózu s hromaděním poškozených mitochondrií, poruchou buněčné signalizace, homeostázy vápníku a indukcí buněčné smrti (3, 17, 22). V současnosti je známých 7 klinických typů MPS lišících se genetickou příčinou, biochemickým podkladem a klinickou manifestací (tab. 1). Jedná se o onemocnění autozomálně recesivně dědičná s výjimkou MPS II s dědičností vázanou na chromozom X (6). Jde o onemocnění vzácná, incidence MPS v České republice je 1 : 26 882 narozených dětí (26).
Postižení v oblasti hlavy a krku je u pacientů s MPS velice časté. Mnohdy se přitom jedná o první manifestaci onemocnění již v časném věku (20, 30). Důvody návštěvy ORL lékaře jsou obdobné jako v ostatní populaci. Jedná se především o recidivující infekce horních dýchacích cest, obstrukci horních dýchacích cest zejména z důvodu adenotonzilární hypertrofie a otologické postižení (recidivující akutní otitida, sekretorická otitida, porucha sluchu) (21, 27, 28). Otorinolaryngolog tak může být prvním specialistou, ke kterému je dítě s MPS odesláno (21). Hraje důležitou roli jak ve včasném rozpoznání nemoci a v iniciaci dalšího vyšetření vedoucího k diagnostice onemocnění, tak i v následném sledování pacientů a v jejich léčbě (14, 27, 30). Cílem této práce je blíže obeznámit otorinolaryngologickou obec s touto vzácnou skupinou onemocnění.
2. SYSTÉMOVÉ POSTIŽENÍ U MUKOPOLYSACHARIDÓZ
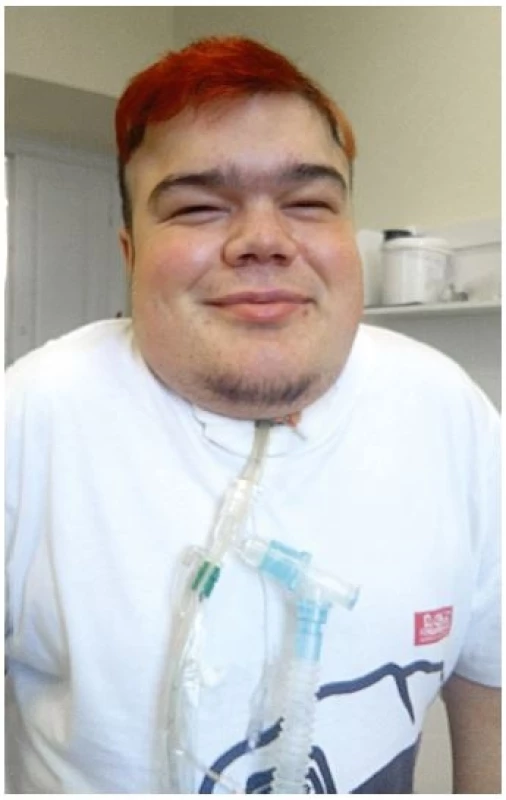
Mukopolysacharidózy jsou onemocnění multisystémová a progresivní, jejich klinická variabilita je široká (17, 30). Manifestují se již v kojeneckém nebo batolecím věku, a to nespecifickými příznaky, např. pupeční nebo tříselní kýlou, hepato - a splenomegalií, větším obvodem hlavy, recidivujícími záněty horních dýchacích cest a středouší, nebo poruchou sluchu. Pro rozvinuté onemocnění jsou pak typické hrubší rysy obličeje s klenutým čelem, prominujícími nadočnicovými oblouky, širokým kořenem nosu, hypertelorismem, antevertrovanými nostrilami a plnými rty (obr. 1). Dále jsou přítomné kratší nosní průchody a makroglosie, které spolu s hypertrofií adenoidních vegetací a tonzilární tkáně souvisejí s rozvojem chronické rýmy, hlasitým dýcháním, ronchopatií a opakovanými záněty středouší (17). Mohou být přítomné tvarové změny zubů, široké uložení zubů, gingivální hyperplazie, hluboký a chraplavý hlas a u některých typů (I, IV, VI) zákal rohovky (17, 30). Hepatomegalie a splenomegalie je vyjádřena hlavně u typů I, II a VI. Z důvodu střádání GAG na srdečních chlopních dochází k rozvoji chlopenních vad a sekundárně i ke kardiomyopatii. Přítomna bývá kombinovaná obstrukční i restrikční plicní porucha. Na rozvoji restrikční poruchy se podílí přítomnost malého hrudního koše s abnormálně tvarovanými žebry a omezená pohyblivost bránice podmíněná zvětšením sleziny a jater (23). Ke vzniku obstrukční poruchy dochází střádáním GAG v sliznici dolních dýchacích cest a přítomnosti abnormalit tracheobronchiálního stromu (5, 23). Kůže může být zhrubělá, s hypertrichózou, hustým obočím a nižší vlasovou hranicí. Téměř vždy je přítomné postižení skeletu, jehož odpovídající rentgenový nález se označuje jako dysostosis multiplex (turecké sedlo v tvaru J, deformity obratlů v ovoidním tvaru, ventrálně se rozšiřující žebra, pánev ve tvaru srdce, dysplázie kyčelních kloubů) (15). Typický pro MPS je syndrom karpálního tunelu (v dětském věku se při jiných diagnózách prakticky nevyskytuje), vývoj kontraktur malých a velkých kloubů s omezením jemné a hrubé motoriky a častým rozvojem drápovité ruky. Pro těžké formy MPS typu I, II a III je typické opoždění a regres vývoje, který se ale naopak nevyskytuje u MPS typu IV a VI (17). Psychiatrická symptomatologie s poruchami chování (agresivita, hyperaktivita, afektivní záchvaty, střídání emocí) je typická pro MPS typu II a III (28). U těžkých forem MPS I., II. a VI. typu může taky dojít k rozvoji hydrocefalu a epilepsie. Všechny uvedené příznaky se rozvíjejí postupně a u malého dítěte nebývají ještě plně vyjádřeny. Klíčem k diagnóze je tak rozpoznání kombinace často zdánlivě nesouvisejících příznaků.§
Publikováno se souhlasem pacienta.
3. OTOLOGICKÁ PROBLEMATIKA
3.1 Akutní a sekretorická otitida
U pacientů s MPS dochází ke střádání GAG v adenoidní tkání, v sliznici retronazálního prostoru, Eustachovy trubice a středního ucha. Tyto změny spolu s dysfunkcí Eustachovy trubice v důsledku kraniofaciálních abnormalit přispívají k rozvoji recidivující akutní otitidy a vývoji sekretorické otitidy (8, 28). Zánět středouší (akutní nebo chronický) je spolu s poruchou sluchu nejčastějším ORL příznakem. V souboru 554 pacientů s MPS II v mezinárodní observační studii HOS (Hunter Outcome Survey) byl přítomen u 72 % pacientů (14).
Vzhledem k progresivnímu charakteru onemocnění je často nutné opakované zavedení ventilačních trubiček, přičemž u mnoha dětí jsou tyto zavedeny ještě před stanovením základní diagnózy (27, 30). Snahou je minimalizovat množství výkonů v CA a zvolit vhodný typ ventilačních trubiček (T tube apod.) s předpokladem delší funkčnosti. V případě nemožnosti provedení operačního výkonu je ke zvážení indikace sluchové protetiky (28). Přístup „watch and wait“ není u pacientů s MPS úspěšný a není proto doporučován (21). U pacientů s MPS II byly ventilační trubičky zavedeny v 50 % (14). U nejtěžší formy MPS I (syndrom Hurlerové) myringotomii a zavedení ventilačních trubiček podstoupilo 57 % pacientů (2). Tympanostomie je tak vůbec nejčastějším chirurgickým zákrokem u této skupiny pacientů (2, 19).
3.2 Porucha sluchu
Porucha sluchu je u dětí s MPS častá. Jedná se typicky o smíšenou nedoslýchavost (25, 28), která obvykle progreduje (1). Má jednoznačný dopad na vývoj řeči a kvalitu života (30). Při vstupu do registru HOS mělo poruchu sluchu 67 % pacientů s MPS II, přičemž se jednalo o druhý nejčastější příznak z ORL oblasti. Při pozdějším hodnocení audiogramů (83 audiogramů od 162 pacientů v HOS) byla podle kritérií WHO přítomná porucha sluchu až u 84 % pacientů (14). Nejčastěji, u 31 % pacientů, byla zastoupená středně těžká porucha sluchu. Lehká a těžká porucha byla potvrzena u 24 %, resp. 22 % pacientů. Velmi těžká porucha sluchu byla diagnostikována v 7 %. Nejčastěji se jednalo o smíšenou a senzorineurální poruchu sluchu (obě 33 %), pak o převodní a variabilní poruchu sluchu (16 % a 18 %). Dle audiometrických měření se kostní práh sluchu zvyšuje přibližně o 1 dB za rok a procento pacientů s oboustrannou poruchou sluchu věkem stoupá, což potvrzuje progresivní charakter senzorineurální komponenty jako přirozené součásti MPS (14).
Tato data odpovídají údajům dalších autorů. Wold uvádí přítomnost různého stupně poruchy sluchu u 7 z 9 pacientů s MPS. Z toho v pěti případech šlo o poruchu smíšenou, po jednom pak senzorineurální a převodní poruchu sluchu (30). V retrospektivní studii publikované Mesolellou (celkem 20 pacientů s MPS) byla porucha sluchu přítomná u 15 pacientů (75 %). Ve 43 % se jednalo o smíšenou poruchu sluchu, ve 43 % o převodní a v 13 % o senzorineurální poruchu sluchu (20).
Na začátku onemocnění je porucha sluchu často nejprve jen převodní. Tato je typicky připisována dysfunkci Eustachovy trubice, přítomnosti chronického sekretu ve středouší a rekurentní akutní otitidě (24). Roli může hrát i přítomnost depozitů GAG ve středním uchu a v jeho strukturách (28, 30). V literatuře byly popsané i tympanomastoidální abnormality, jako výrazná absence mastoidální pneumatizace, vyplň středního ucha fibrózní tkání, 3 - 4x více zhrubělá tympanická membrána. Jedná se nejspíše o následek chronické otitidy, ale diskutována je i porucha fetálního vývoje (9).
Později se s progresí nemoci může vyvinout porucha smíšená se senzorineurální složkou (14). Patofyziologie rozvoje senzorineurální poruchy sluchu není dostatečně objasněna (21, 28). Zvažována je opět kongenitální porucha nebo sekundární podmínění střádáním parciálně degradovaných GAG ve strukturách vnitřního ucha (ductus chochlearis, stria vascularis), n. VIII nebo v CNS (7).
Progresivní povaha poruchy sluchu vyžaduje opakované audiologické vyšetření. Zlepšení sluchu po chirurgické léčbě (zavedení ventilačních trubiček) bylo pozorováno u 60 % pacientů (20). Kromě drenáže středouší je možností léčby také použití sluchadel, ale u pacientů s vážnými behaviorálními potížemi není jejich přínos dostatečný (21).
4. OBSTRUKCE DÝCHACÍCH CEST
4.1 Adenotonzilární hypertrofie
Z důvodu ukládání GAG v lymfatické tkáni hltanu a faryngální stěně je adenotonzilární hyperplázie velmi častým nálezem. Ve spojení s makroglosií a mandibulárními abnormalitami je u pacientů s MPS vyšší riziko vzniku progresivní obstrukce HCD a syndromu obstrukční spánkové apnoe (28). Např. Mesolella popisuje obstrukci HCD u patnácti z dvaceti pacientů s MPS. K hypertrofii lymfatické tkáně hltanu mohou také přispívat i opakované infekce horních dýchacích cest.
Z léčebných modalit se v řešení obstrukce dýchacích cest iniciálně provádí adenotonzilektomie, která je v mnoha případech dostačující (28). Podle údajů HOS je u pacientů s MPS II adenotomie druhou nejčastější ORL intervencí (47 % pacientů) (14), následována tonzilektomií (35,5 % pacientů) (19). Dle mezinárodního registru pro pacienty s MPS I je adenotonzilektomie třetím nejčastějším chirurgickým výkonem (37 % pacientů se syndromem Hurlerlové) (2). Wold v retrospektivní studii uvádí klinicky signifikantní obstrukci HCD u čtyř pacientů z devíti a symptomatické zlepšení po adenotozilektomii u všech pacientů (30). U pacientů, u kterých je tento zákrok nepostačující nebo obstrukce dýchacích cest progreduje, je indikována dechová podpora (nazální CPAP), v extrémních případech může být nutná i tracheotomie (28). Při provádění adenotonzilektomie je nutné myslet na potenciální krční instabilitu, která je kontraindikací záklonu hlavy u těchto pacientů (anesteziologická rizika viz. dále).
4.2 Progresivní obstrukce dýchacích cest
Případy zbytnělé tkáně jsou popsány rovněž v laryngu nad arytenoidními chrupavkami a aryepiglotickými řasami. Tyto mohou prolabovat se vznikem stridoru a těžké obstrukce dýchacích cest (28). K malácii a kolapsibilitě dochází rovněž na úrovni trachey a bronchů. V těchto případech se doporučuje provedení diagnostické a eventuálně terapeutické laryngotracheobronchoskopie. Někdy je k zajištění dýchacích cest nutná tracheotomie spolu se zvážením zavedení tracheálního stentu.
5. DIAGNOSTIKA A LÉČBA MUKOPOLYSACHARIDÓZ
Diagnostika mukopolysacharidóz je náročná a vzhledem k podobnosti s jinými dědičnými metabolickými poruchami by měla probíhat na specializovaném pracovišti. Při klinickém podezření se odesílá kvantitativní stanovení GAG v moči. Při zvýšené exkreci GAG se dále provádí elektroforetické vyšetření s rozdělením GAG na jednotlivé frakce (17). K určení jednotlivých typů mukopolysacharidóz na biochemické úrovni je potřebné stanovit aktivitu jednotlivých enzymů v izolovaných leukocytech, v buněčné kultuře kožních fibroblastů nebo v suché krevní kapce. Definitivní diagnóza je potvrzena molekulárně-genetickým vyšetřením. Přestože většina dětí je diagnostikována mezi 3.–4. rokem života, první příznaky onemocnění jsou obvykle přítomné mnohem dříve (18). Průměrná doba mezi objevením se prvního příznaku a stanovením diagnózy je 2,4 roku (0-9 let) (6).
V léčbě MPS je v současné době k dispozici několik léčebných modalit. Spolu se symptomatickou léčbou je vysoká snaha léčit tento patologický proces jako celek, s cílem předejít rozvoji jednotlivých symptomů, nebo alespoň zpomalit progresi onemocnění (30).
Transplantace kostní dřeně se používá od r. 1980 a indikuje se často u dětí s MPS typu I se závažnou formou onemocnění nebo u dětí s mírnou formou MPS typu VI a VII (30). Dlouhodobá data poukazují na redukci hepatosplenomegalie, zlepšení obstrukce dýchacích cest, stabilizaci mentálního postižení. Ke zlepšení dochází pravděpodobně obnovením schopnosti degradovat akumulované substráty na buněčné úrovni (4, 11, 29). V ORL oblasti se předpokládá zlepšení sluchu a hlasu ve srovnání s pacienty bez léčby, i když Papsin uvádí, že smíšená porucha sluchu je přítomna i u pacientů po úspěšné transplantaci (25).
Významnou změnu v léčbě dětí s MPS představuje zavedení enzymové substituční terapie (Enzyme Replacement Therapy, ERT), která je momentálně dostupná pro MPS typu I, II, IV a VI. Spočívá v podávání rekombinantně připraveného enzymu ve formě nitrožilní infuze jednou týdně nebo jedenkrát za dva týdny. Obecně je léčba dobře tolerována a závažné nežádoucí účinky se vyskytují jen vzácně (16). ERT zlepšuje funkci postižených orgánů, zmírňuje množství příznaků, zpomaluje progresi onemocnění a zlepšuje kvalitu života pacientů (15). Ovlivňuje zejména parenchymatózní, dobře vaskularizované orgány–játra a slezinu, stabilizuje plicní funkce a progresi srdečního postižení. Z důvodu neschopnosti přestupu rekombinantního enzymu přes hematoencefalickou bariéru nemá ERT vliv na postižení CNS (10) a je také špatně účinná u postižení skeletu, chrupavky a srdečních chlopní.
Zásadní pro úspěšnost ERT i transplantace kostní dřeně je včasnost stanovení diagnózy a zahájení léčby (30). Studie na sourozeneckých párech, kdy byl mladší sourozenec diagnostikován a léčen na základě diagnózy staršího sourozence dokumentují, že při zahájení léčby v presymtomatickém stadiu lze mnoha patologickým orgánovým projevům i zcela předejít (12, 13).
Důležité postavení v péči o pacienty s MPS má léčba symptomatická, fyzioterapie, chirurgická léčba (operace pupečních a tříselních kýl, ORL operace), ortopedické výkony (řešení útlaku krční míchy, hydrocefalu, operace syndromu karpálního tunelu). Nezbytná pro pacienty a jejich rodiny je psychoterapeutická podpora. Léčba dosahuje lepších výsledků, pokud je zahájená v nižším věku nebo před progresí nemocí (30). Součástí diagnostického postupu je genetické poradenství, vypracování rodokmenu a identifikace členů rodiny s možným rizikem přenašečství (16).
6. POZNÁMKY K ANESTEZII PACIENTŮ S MUKOPOLYSACHARIDÓZOU
Z anesteziologického hlediska patří pacienti s MPS k nejrizikovější skupině, zejména pro obtížné zajištění dýchacích cest a multisystémové postižení většiny orgánů z nastřádaných GAG. Zásadní pro podání anestezie je postižení dýchacího systému, srdce, CNS a skeletu.
Na obstrukci horních dýchacích cest se podílejí krátký krk, limitované otevření úst (temporomandibulární ankylóza), zbytnění faryngeálních sliznic, včetně adenotonzilární hyperplázie, excesivní sekrece, makroglosie a abnormální anatomie hrtanu, např. laryngomalacie (29). V dolních dýchacích cestách zvyšují riziko obstrukce subglotická stenóza, tracheomalácie, obstrukční změny plicního parenchymu (chronický zánět, atelektázy, plicní hypertenze až cor pulmonale) a restrikční plicní postižení (deformity hrudníku a páteře-hrudní kyfóza, protruze sterna, gibus). Významné je postižení krční páteře s možnou atlantookcipitální instabilitou a rizikem subluxace krčních obratlů s akutním útlakem míchy a kvadruplegií. Incidence atlantookcipitální instability je vysoká téměř u všech pacientů s MPS IV a u některých s MPS I, II a VI. Další riziko představuje postižení kardiovaskulárního systému. U většiny pacientů vznikají patologické změny na chlopních (aortální nebo mitrální stenóza či insuficience). Dilatace srdce až městnavé srdeční selhání hrozí také na podkladě kardiomyopatie.
Před podáním celkové anestezie se zaměřujeme na důslednou anesteziologickou anamnézu (předchozí operace a průběh anestezie). Vzhledem k multisystémovému postižení by předanestetické vyšetření mělo obsahovat podrobné pediatrické vyšetření, včetně vyšetření srdce (nutnost podání antibiotické prevence, CNS (hydrocefalus, psychomotorická retardace), krční páteře (MRI) a dýchacího systému (spirometrie).
Z výše uvedených příčin je pro pacienty s MPS nejrizikovější úvod do celkové anestezie, zejména pak zajištění dýchacích cest. Kombinace selhání ventilace přes obličejovou masku, kardiálního postižení a obtížné intubace může vést i k náhlému úmrtí. Incidence ztížené intubace se u dětí s MPS udává až 25% (29). Při zajišťování dýchacích cest je kontraindikován záklon hlavy, přednostně dýchací cesty zajišťujeme laryngeální maskou. V případě nutnosti intubace volíme techniku fibrooptické intubace v inhalační anestezii sevofluranem se zachovanou spontánní ventilací. Vhodná je kombinace s lokální anestezií horních dýchacích cest a vchodem do hrtanu. V případě selhání předchozích technik je na místě provedení tracheotomie. Pacienty monitorujeme jak po podání sedace v premedikaci (např. Midazolam max.0,2 mg/kg), tak i po podání celkové anestezie pro možnou obstrukci dýchacích cest v pooperačním období.
Anestezii u pacientů s MPS by měl podávat zkušený anesteziolog vybavený potřebnými pomůckami pro obtížné zajištění dýchacích cest i u zdánlivě banálních operačních zákroků jako je inzerce tympanostomických trubiček nebo adenotonzilektomie. Zároveň i operační zákrok by měl provádět zkušený operatér z důvodu maximální eliminace možných komplikací a nutností podání další anestezie.
ZÁVĚR
Postižení v ORL oblasti je u pacientů s MPS velice časté. Otorinolaryngologické vyšetření, mnohdy i chirurgická intervence, často diagnóze MPS předchází. Otorinolaryngolog tak hraje důležitou roli ve včasném rozpoznání nemoci, v iniciaci dalšího vyšetření vedoucího k diagnostice onemocnění a v následném sledování a léčbě pacientů. K podezření na diagnózu vede zejména kombinace příznaků u pacienta, např. přítomnost sekretorické otitídy, tříselné kýly, hrubších rysů obličeje nebo opožděného vývoje. Péče o tyto pacienty vyžaduje multidisciplinární tým a vzhledem k své náročnosti by měla být koncentrovaná do specializovaných center.
Tato práce vznikla za podpory projektu UK v Praze UNCE 204064, PROGRES Q26/LF1 a RVO-VFN 64165/2012.
Adresa ke korespondenci:
Doc. MUDr. Martin Magner, Ph.D.
Klinika dětského a dorostového lékařství
1. LF UK a VFN
Ke Karlovu 2
128 08 Praha 2
e-mail: martin.magner@vfn.cz
Sources
1. Al Sawaf, S., Mayatepek, E., Hoffmann, B.: Neurological findings in Hunter disease: pathology and possible therapeutic effects reviewed. J. Inherit. Metab. Dis., 31, 2008, 4, s. 473-480.
2. Arn, P., Wraith, J. E., Underhill, L.: Characterization of surgical procedures in patients with mucopolysaccharidosis type I: Findings from MPS I Registry. J. Pediatr., 154, 2009, 6, s. 859-864.
3. Beck, M.: Therapy for lysosomal storage disorders. IUBMB Life, 62, 2010, 1, s. 33-40.
4. Belani, K. G., Krivit, W., Carpenter, B. L. J. et al.: Children with mucopolysaccharidosis: perioperative care, morbidity, mortality, and new findings. Pediatr. Surg., 28, 1993, 3, s. 403-408.
5. Berger, K. I., Fagondes, S. C., Giugliani, R. et al.: Respiratory and sleep disorders in mucopolysaccharidosis. J. Inherit. Metab. Dis., 36, 2013, 2, s. 201-210.
6. Dvorakova, L., Vlaskova, H., Sarajlija A. et al.: Genotype–phenotype correlation in 44 Czech, Slovak, Croatian and Serbian patients with mucopolysaccharidosis type II. Clin. Genet., 91, 2017, 5, s. 787-796.
7. Friedmann, I., Spellacy, E., Crow, J. et al.: Histopathological studies of the temporal bones in Hurles´s disease (mucopolysaccharidosis IH), J. Laryngol. Otol., 99, 1985, 1, s. 29-41.
8. Gönüldaş, B., Yılmaz, T., Sivri, H. S. et al.: Mucopolysaccharidosis: Otolaryngologic findings, obstructive sleep apnea and accumulation of glucosaminoglycans in lymphatic tissue of the upper airway. Int. J. Pediatr. Otorhinolaryngol., 78, 2014, 6, s. 944-949.
9. Hayes, E., Babin, R., Platz, C.: The otologic manifestations of mucopolysaccharidoses. Am. J. Otol., 2, 1980, 2, s. 65-69.
10. Hendriksz, C. J., Burton, B., Fleming T. R. et al.: Efficacy and safety of enzyme replacement therapy with BMN 110 (elosulfase alfa) for Morquio A syndrome (mucopolysaccharidosis IVA): a phase 3 randomised placebo‑controlled study. J. Inherit. Metab. Dis., 37, 2014, 6, s. 979-990.
11. Hopwood, J. J., Vellodi, A., Scott, H. S. et al.: Long-term clinical progress in bone marrow transplanted mucopolysaccharidosis type I patients with a defined genotype. J. Inherit. Metab. Dis., 16, 1993, 6, s. 1024-1033.
12. Jurecka, A., Malinova, V., Tylki Szymańska, A.: Effect of rapid cessation of enzyme replacement therapy: a report of 5 more cases. Mol. Genet. Metab., 111, 2014, 2, s. 212–213.
13. Jurecka, A., Żuberuber, Z., Opoka Winiarska, V. et al.: Effect of rapid cessation of enzyme replacement therapy: a report of 5 cases and a review of the literature. Mol. Genet. Metab., 107, 2012, 3, s. 508-512.
14. Keilmann, A., Nakarat, T., Bruce, I. A. et al..: Hearing loss in patients with mucopolysaccharidosis II: Data from HOS – the Hunter Outcome Survey. J. Inherit. Metab. Dis., 35, 2012, 2, s. 343-353.
15. Kulhánek, J., Malinová, V., Honzík, T. et al.: Enzymová substituční terapie u lysosomálních onemocnění. Čes. Slov. Pediat., 70, 2015, 4, s. 224-231.
16. Kulhánek, J., Albrecht, J., Honzík, T. et al.: Psychiatrická manifestace dědičných metabolických poruch. Čes. Slov. Psychiat., 111, 2015, 6, s. 295-305.
17. Magner, M., Kulhánek, J., Zeman, J.: Enzymová substituční terapie pacientů s mukopolysacharidózami. Remedia, 26, 2016, 4, s. 1-5.
18. Meikle, P. J., Hopwood, J. J., Clague A. E. et al.: Prevalence of lysosomal storage disorders. JAMA, 281, 1999, 3, s. 249-254.
19. Mendelsohn, N. J., Harmatz, P., Bodamer, O. et al.: Importance of surgical history in diagnosing mucopolysaccharidosis type II (Hunter syndrome): Data from the Hunter Outcome Survey. Genet. Med., 12, 2010, 12, s. 816-822.
20. Mesolella, M., CiMMino, M., Cantone, E. et al.: Management of otolaryngological manifestations in mucopolysaccharidoses: our experience. Acta Otorhinolaryngol. Ital., 33, 2013, 4, s. 267-272.
21. Motamed, M., Thorne, S., Narula, A.: Treatment of otitis media with effusion in children with mucopolysaccharidoses. Int. J. Pediatr. Otorhinolaryngol., 53, 2000, 2, s. 121-124.
22. Menze, J.: Early initiation of enzyme replacement therapy for mucopolysaccharidoses. Mol. Genet. Metab., 111, 2014, 2, s. 63-72.
23. Muenzer, J., Wraith J. E., Clarke, L. A.: Mucopolysaccharidosis I: Management and Treatment Guidelines. Pediatrics, 123, 2009, 1, s. 19-29.
24. Napiontek, U., Keilmann, A.: Hearing impairment in patients with mucopolysaccharidoses. Acta Paediatrica Suppl., 451, 2006, 1, s.113-117
25. Papsin, B. C., Vellodi, A., Bailey, C. M. et al.: Otologic and laryngeal manifestations of mucopolysaccharidoses after bone marrow transplantation. Otolaryngol. Head Neck Surgery., 118, 1998, 1, s. 30-36.
26. Poupětová, H., Ledvinová, J., Berná, L. et al.: The birth prevalence of lysosomal storage disorders in the Czech Republic: comparison with data in different populations. J. Inherit. Metab. Dis., 33, 2010, 4, s. 387–396.
27. Ruckenstein, M. J., Macdonald, R. E., Clarke, J. et al: The management of otolaryngological problems in the mucopolysaccharidoses: a retrospective review, J. Otolaryngol., 20, 1991, 3, s. 177-183.
28. Simmons, M. A., Bruce, I. A., Penney, S. et al: Otorhinolaryngological manifestations of the mucopolysaccharidoses. Int. J. Pediatr. Otorhinolaryngol., 69, 2005, 5, s. 589-595.
29. Walker, R., Darowski, M., Morris, P. et al.: Anaesthesia and mucopolysaccharidoses: a review of airway problems in children, Anaesthesia., 49, 1994, 12, s. 1078-1084.
30. Wold, S. M., Derkay, C. S., Darrow, D. H. et al.: Role of the pediatric otolaryngologist in diagnosis and management of children with mucopolysaccharidoses. Int. J. Pediatr. Otorhinolaryngol., 74, 2010, 1, s. 27-31.
Labels
Audiology Paediatric ENT ENT (Otorhinolaryngology)Article was published in
Otorhinolaryngology and Phoniatrics

2018 Issue 3
-
All articles in this issue
- Endoskopická resekce juvenilního angiofibromu nosohltanu
- Role audiologických metod v diagnostice lézí mostomozečkového koutu
- Spontánní sublinguální hematom jako manifestace získané hemofilie
- Silent sinus syndrom
- Mukopolysacharidózy z pohledu otorinolaryngologa
- Přehled implantátů pro kostní vedení a aktivních středoušních implantátů
- Rekonstrukce lícního nervu po resekčních výkonech parotiché žlázy: Ausa cervicalis hypoglosso faciální anastomóza
- Otorhinolaryngology and Phoniatrics
- Journal archive
- Current issue
- About the journal
Most read in this issue
- Přehled implantátů pro kostní vedení a aktivních středoušních implantátů
- Spontánní sublinguální hematom jako manifestace získané hemofilie
- Silent sinus syndrom
- Role audiologických metod v diagnostice lézí mostomozečkového koutu
