Peroperační využití potencované kontaktní endoskopie k hodnocení maligního potenciálu slizničních lézí hrtanu, validace ELS klasifikace
Intraoperative use of enhanced contact endoscopy for evaluation of laryngeal mucosal lesions, validation of ELS classification
Introduction: Enhanced contact endoscopy (ECE) – combination of contact endoscopy and NBI (narrow-band imaging) or IMAGE1 S, is a non-invasive optical technique used for assessment of superficial vascular changes of mucosal lesions in high magnification. Aim: The aim of our study was to evaluate the diagnostic value of ECE in an intraoperative settlement and validation of the ELS classification. Methods: Patients with laryngeal lesions underwent direct laryngoscopy with a structured assessment of the lesion using white light, NBI and ECE. Lesions were classified according to the European Laryngological Society Classification that divides the vascular pattern changes into longitudinal (unsuspicious) and perpendicular (suspicious). Evaluation was correlated with histopathology. Results: 60 patients with 76 lesions were enrolled. Sensitivity, specificity, positive predictive value (PPV), negative predictive value (NPV) and accuracy for NBI assessment reached 71.4%, 100%, 100%, 53.8% and 78.6%, resp., k index of 0.556. Sensitivity, specificity, PPV, NPV and accuracy for ECE reached 86.4%, 89.5%, 95.0%, 73.9% and 87.3%, k index of 0.716. Additional 20% (9/45) of the leukoplakias could be assessed with ECE compared to NBI. Conclusions: Our data support the assumption that ECE is a useful tool for pre-histological examination of mucosal lesions, however it cannot fully replace biopsy sampling. ECE shows higher accuracy in detecting malignant lesions compared to NBI and can be especially helpful in the assessment of vocal fold leukoplakia.
Keywords:
squamous cell carcinoma – enhanced contact endoscopy – narrow-band imaging – laryngeal mucosal lesions – leukoplakia
Autoři:
Anna Švejdová 1,2
; Michal Homoláč 1,2
; Peter Kántor 3,4
; Michal Černý 1,2
; Jana Šatanková 1,2
; Lucie Zeinerová 1
; Jan Mejzlík 1,2
; Jana Krtičková 1,2
; Viktor Chrobok 1,2
Působiště autorů:
Klinika otorinolaryngologie a chirurgie hlavy a krku, FN Hradec Králové
1; Univerzita Karlova, LF v Hradci Králové
2; Klinika otorinolaryngologie a chirurgie hlavy a krku, FN Ostrava
3; Katedra kraniofaciálních oborů, LF OU, Ostrava
4
Vyšlo v časopise:
Otorinolaryngol Foniatr, 73, 2024, No. 1, pp. 28-36.
Kategorie:
Původní práce
doi:
https://doi.org/10.48095/ccorl202428
Souhrn
Úvod: Potencovaná kontaktní endoskopie (ECE), kombinace kontaktní endoskopie (CE) a narrow-band imaging (NBI) či IMAGE1 S patří mezi neinvazivní optické metody. Využívá se pro hodnocení slizničních lézí na základě změn vaskularizace pomocí velkého optického zvětšení. Cíl: Cílem práce bylo zhodnocení diagnostického přínosu peroperačního využití ECE pro hodnocení slizničních lézí hrtanu a validace ELS klasifikace. Metodika: Do studie byli zařazeni pacienti se slizničními lézemi hrtanu, kteří podstoupili přímou laryngoskopii v celkové anestezii. Léze byly postupně hodnoceny na základě strukturovaného vyšetření v bílém světle, NBI a ECE a zhodnoceny dle klasifikace Evropské laryngologické společnosti (ELS klasifikace) jako nesuspektní (longitudinální vaskularizace), nebo suspektní (perpendikulární vaskularizace). U všech pacientů byla provedena biopsie a histologické vyšetření. Výsledky klasifikovaných lézí byly korelovány s histologickým vyšetřením. Výsledky: Celkově bylo vyšetřeno 60 pacientů se 76 lézemi. Senzitivita, specificita, pozitivní prediktivní hodnota (PPV), negativní prediktivní hodnota (NPV) a správnost pro NBI dosáhla 71,4 %, 100 %, 100 %, 53,8 % a 78,6 %, k index 0,556. Senzitivita, specificita, PPV, NPV a správnost pro ECE dosáhla 86,4 %, 89,5 %, 95,0 %, 73,9 % a 87,3 %, k index 0,716. Díky těsnému kontaktu se sliznicí při vyšetření ECE bylo oproti samotnému NBI možné zobrazit a hodnotit v ECE o 20 % (9/45) lézí charakteru leukoplakií navíc. Závěr: Naše data potvrzují, že potencovaná kontaktní endoskopie je přínosným nástrojem pro předhistologické vyšetření slizničních lézí hrtanu, avšak nemůže plně nahradit bioptickou verifikaci, jejím limitem jsou především těžce dosažitelné léze (např. dolní plocha hlasivky) a hyperkeratóza. Ve srovnání s NBI je ECE přesnější, díky velkému zvětšení může být zvláště přínosná pro hodnocení některých leukoplakií.
Klíčová slova:
dlaždicobuněčný karcinom – potencovaná kontaktní endoskopie – narrow-band imaging – slizniční léze hrtanu – leukoplakie
Úvod
Dlaždicobuněčný karcinom hrtanu patří mezi onemocnění s vysokou incidencí (2,76/100 tis.), morbiditou a mortalitou (1,66/100 tis.) [1,2]. Vzniká buď primárně jako invazivní karcinom, nebo na podkladě slizničních lézí – prekanceróz (dysplazií) v rámci několikastupňového procesu transformace z normální sliznice až do stadia karcinomu [3,4]. Stadium záchytu onemocnění je klíčové z hlediska možností terapie a prognózy pacienta. Z tohoto důvodu hraje vyšetření před operačním výkonem zásadní roli, posouzení léze by mělo vést k dostatečnému, ne však k nadbytečnému ošetření. Zároveň je nutné zvažovat mezi radikalitou a rozsahem výkonu na jedné straně a kvalitou života (a hlasu) po chirurgickém výkonu na straně druhé.
Významnou roli v patogenezi nádorových onemocnění představují změny slizniční vaskularizace, podle kterých můžeme posuzovat biologický charakter lézí [5]. Pro předoperační hodnocení maligního potenciálu slizničních změn se v současnosti již standardně využívá zvýraznění slizniční vaskularizace pomocí NBI (narrow-band imaging) či IMAGE1 S, které lze provádět ambulantně při flexibilní laryngoskopii. Peroperačně lze využít další z optických metod – kontaktní endoskopii (CE – contact endoscopy), která umožňuje zobrazení slizniční vaskularizace se zvětšením až 1 100krát (optický zoom 60–150krát + digitální zoom). Metody NBI a CE lze kombinovat, čímž dosáhneme zvýraznění kontrastu a současně výrazného zvětšení pro hodnocení změn slizniční vaskularizace. Metodu pak nazýváme potencovaná kontaktní endoskopie (ECE – enhanced contact endoscopy). Na základě vyšetření ECE lze provádět tzv. předhistologickou diagnostiku a upravit radikalitu výkonu, dále lze ECE využít při cílené biopsii či k zajištění resekčních okrajů. Nevýhodou ECE je, že lze provádět pouze rigidní optikou, a jak vyplývá z názvu metody, je nutný těsný kontakt optické čočky a sliznice, proto je nutné vyšetření v oblasti hrtanu provádět v celkové anestezii. ECE tedy nelze využít v rámci ambulantního sledování.
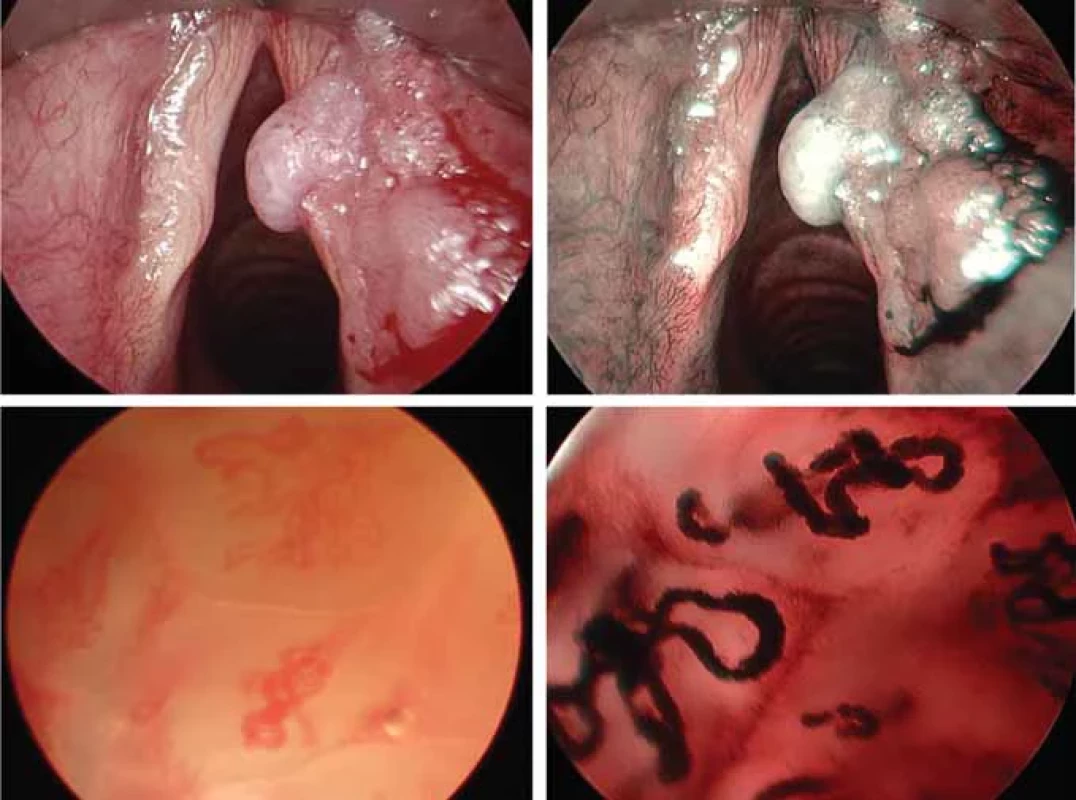
K hodnocení změn vaskularizace se v současnosti využívají tři klasifikace, původně pro NBI byla vyvinuta sedmistupňová klasifikace dle Ni [6] (stupně I–IV, Va, Vb, Vc), pro ECE s využitím IMAGE1S se využívá pětistupňová klasifikace dle Puxeddu et al. [7] (stupně 0–IV), nejčastěji se pro svou jednoduchost využívá dvoustupňová klasifikace navržená Evropskou laryngologickou společností (ELS klasifikace/Arensova klasifikace) [8], která rozděluje změny slizniční vaskularizace na longitudinální a perpendikulární (obr. 1a, b). Longitudinální změny vaskularizace jsou charakteristické tím, že se opticky jeví pouze ve dvou rovinách – cévy mění svou délku a šířku, popisují se jako ektazie, meandry, varikozity, konvoluty, větvení cév apod. Perpendikulární změny vaskularizace postihují hlasivku ve třech rovinách směrem do hloubky, u klasifikace dle Ni je nazýváme intraepiteliální papilární kapilární kličky (IPCLs – intraepithelial papillary capillary loops). Kličky mohou na konci být široké či úzké [8,9]. Mezi onkologicky nesuspektní léze se řadí léze se změnami longitudinálními a perpendikulárními se širokými kličkami – charakteristické pro papilomy (obr. 2a), ostatní perpendikulární změny se řadí mezi onkologicky suspektní léze (obr. 2b).
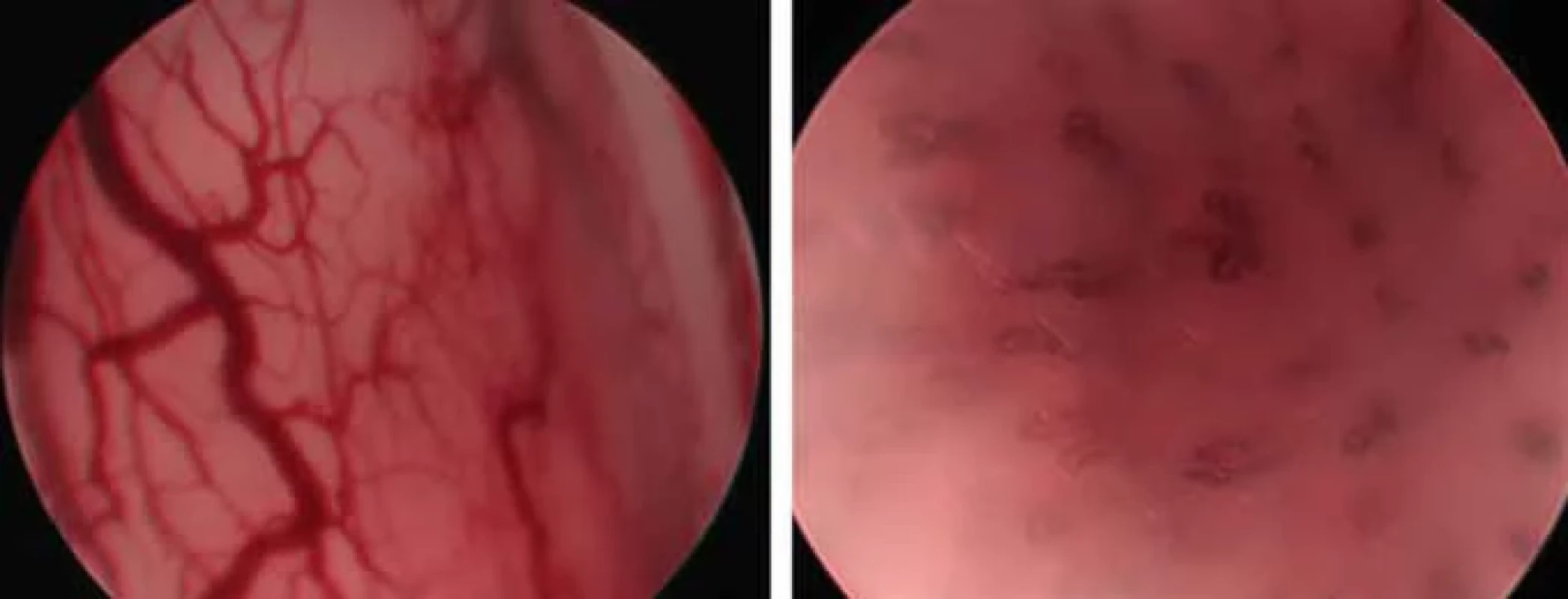
Fig. 1. Longitudinal (A) and perpendicular (B) vascular changes, ECE.
ECE – enhanced contact endoscopy
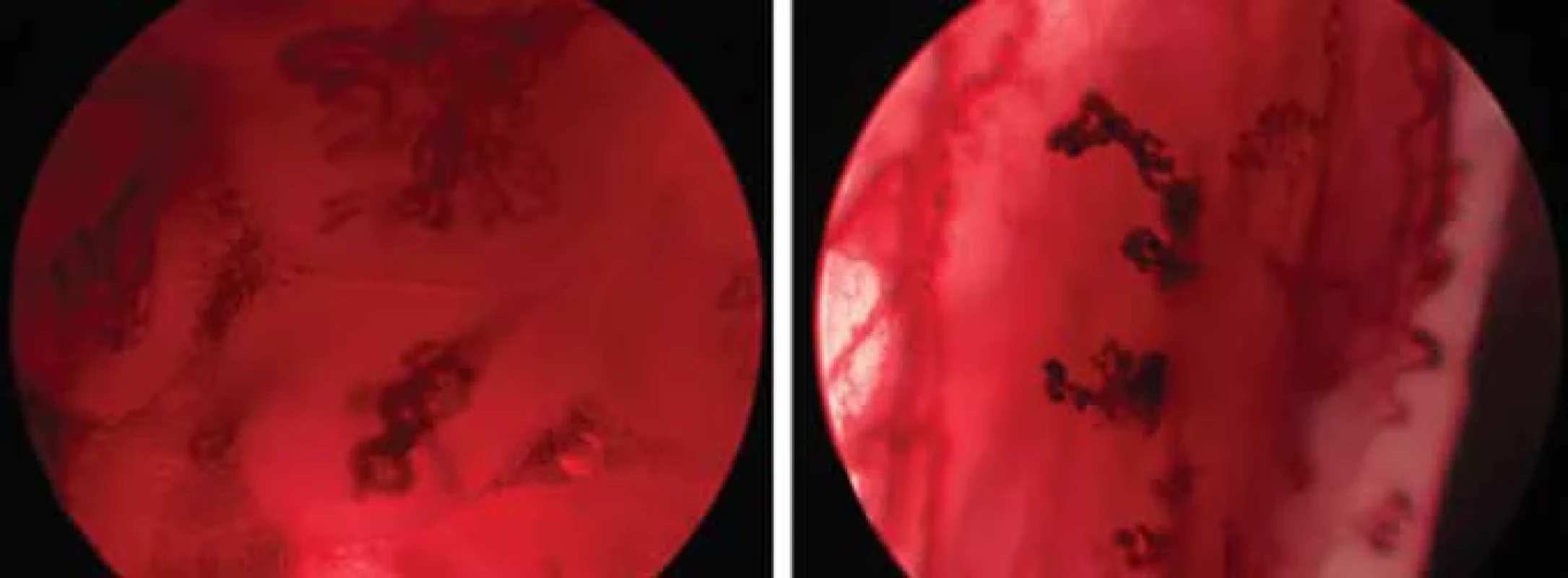
Fig. 2. Perpendicular vascular changes with wide angles (A), narrow angles (B), ECE.
ECE – enhanced contact endoscopy
Metodika
Jedná se o prospektivní klinickou studii na Klinice otorinolaryngologie a chirurgie hlavy a krku ve FN Hradec Králové v období od listopadu 2020 do prosince 2022. Studie byla schválena etickou komisí (202101 P03). Pacienti se slizničními lézemi hrtanu byli nejprve vyšetřeni ambulantně flexibilní laryngoskopií v bílém světle (WLE) a v NBI. Následně v celkové anestezii při direktní laryngoskopii opět v WLE, NBI, poté CE a ECE, léze byly hodnoceny dle ELS klasifikace. Zařazení léze mezi suspektní a nesuspektní jsme prováděli na základě optického vyšetření centra léze, u leukoplakií jsme posuzovali také okraje léze a její okolí. Léze, u nichž se nezdařilo vyšetřit centrum, jsme z hodnocení vyřadili. Hodnocení prováděli čtyři lékaři-specialisté v endoskopické diagnostice, u každého vyšetření byli přítomni vždy společně alespoň dva.
Po vyřazení nehodnotitelných nálezů bylo do studie zařazeno celkem 60 pacientů se 76 slizničními lézemi hrtanu. Po endoskopickém vyšetření lézí se pomocí studených nástrojů nebo CO2 laseru provedlo chirurgické ošetření s odběrem materiálu pro histologické vyšetření. Pokud to bylo z pohledu anesteziologa, pacienta a jeho anatomických poměrů možné, byl výkon proveden v tryskové ventilaci. Výsledky optických metod klasifikovaných dle ELS (NBI a ECE) jsme korelovali s výsledkem histologického vyšetření. Mezi maligní léze jsme dle doporučení ELS zařadili low‑grade dysplazie, high‑grade dysplazie, karcinomy in situ a invazivní karcinomy [8, 9]. Histologické zařazení léze patologem bylo prováděno dle klasifikace WHO z roku 2017, která využívá dvoustupňový systém klasifikace dysplazií (low‑grade a high‑grade) [10, 11].
Z rizikových faktorů jsme sledovali nikotinizmus, užívání alkoholu a extraezofageální reflux.
Přístrojové vybavení
Pacienti byli ambulantně vyšetřeni pomocí HDTV-WLE a HDTV-NBI flexibilním videolaryngoskopem ENF-VQ nebo či ENF-VH připojeným k optickému systému Evis Exera II CLV (Olympus Medical System Corp., Tokyo, Japan). V celkové anestezii HDTV-WLE a HDTV-NBI rigidními kontaktními a nekontaktními endoskopy 0° a/nebo 30° (Karl Storz, Tuttlingen, Germany). Vyšetření jsme zaznamenávali tak, aby bylo možné i zpětně porovnat výsledky optických metod a výsledky histologického vyšetření.
Statistické zpracování
Ke statistickému vyhodnocení byl použit software The Jamovi project (version 2.3) založený na statistickém programovacím jazyku R. Demografické hodnoty zkoumaného souboru pacientů byly vyjádřeny pomocí průměru, mediánu, rozmezí hodnot a směrodatné odchylky (SD). Jednotlivé diagnostické metody byly hodnoceny pomocí senzitivity (SE), specificity (SP), správnosti (ACC – accuracy), pozitivní prediktivní hodnoty (PPV), negativní prediktivní hodnoty (NPV), k indexu, dále byla provedena ROC analýza s vyjádřením hodnoty plochy pod ROC křivkou (AUC). K jednotlivým hodnotám byl také doplněn 95% interval spolehlivosti (CI).

Výsledky
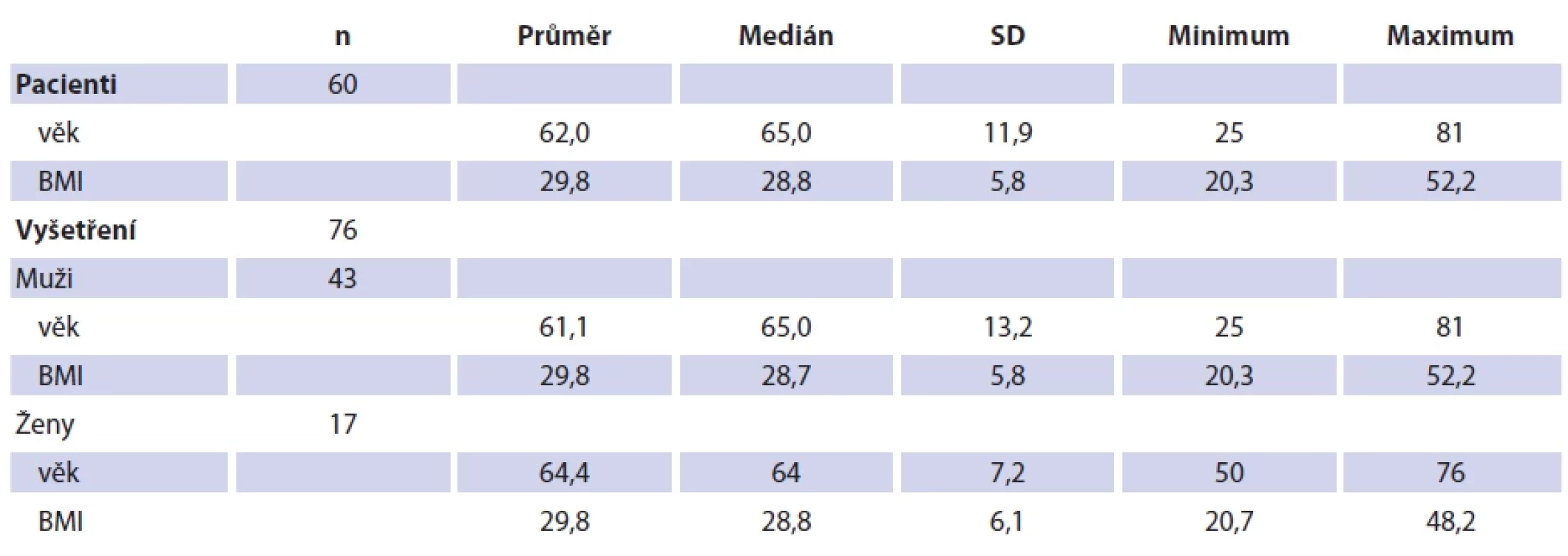
Do souboru bylo celkem zařazeno 60 pacientů se 76 slizničními lézemi hrtanu, 43 mužů a 17 žen, průměrný věk pacientů byl 62,0 let (rozmezí 25–81 let; SD 11,9). Demografická data pacientů jsou zaznamenána v tab. 1. Průměrný body mass index (BMI) u mužů byl 29,8 kg/m2 (SD 5,8), u žen také 29,8 kg/m2 (SD 6,1), nebyl prokázán statisticky významný rozdíl. Neprokázali jsme statistickou významnost BMI ani ve vztahu k dalším rizikovým faktorům – kouření, alkohol, věk, refluxní choroba jícnu.
Nikotinizmus udávalo 75,9 % (44/60) pacientů, pravidelný příjem alkoholu přiznalo 16,7 % (10/60); nicméně příležitostně již 68,3 % (41/60); devět pacientů udávalo, že jsou abstinenti. Refluxní choroba anamnesticky byla zaznamenána u 36,7 % (22/60) pacientů.
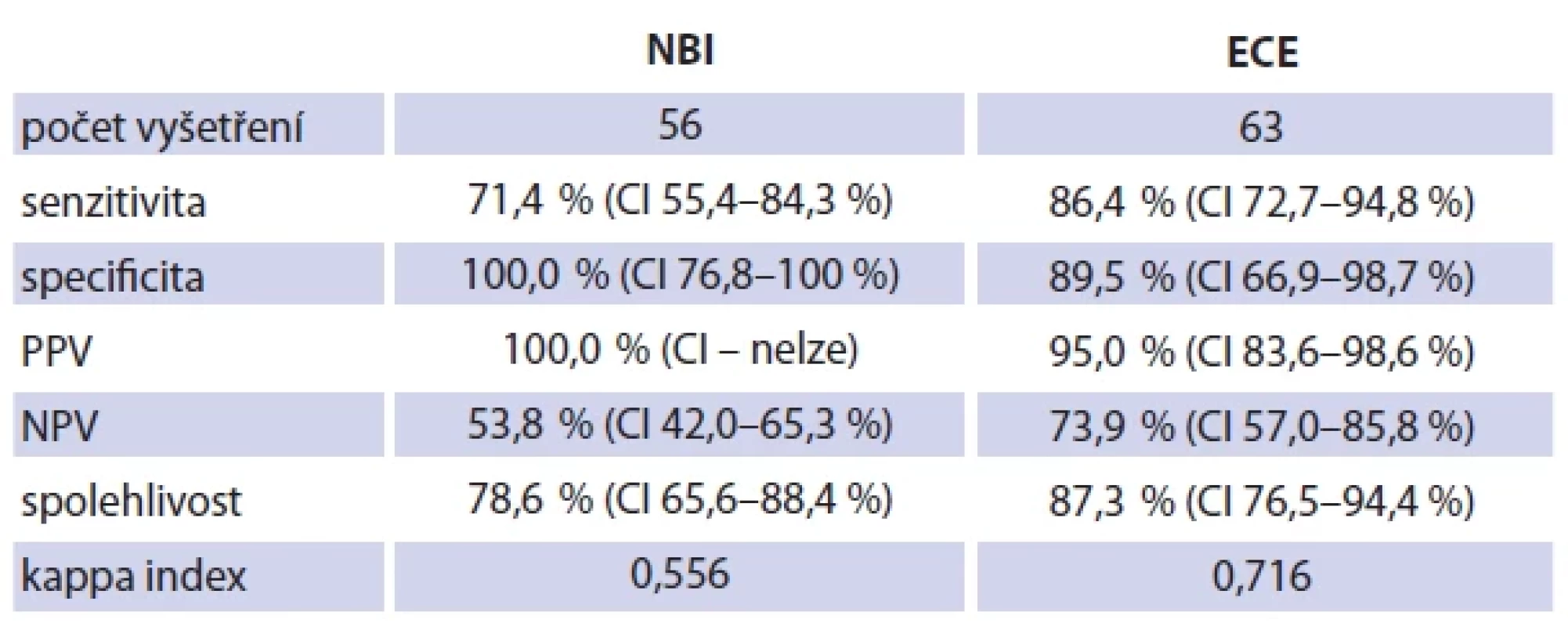
Na základě NBI vyšetření v celkové anestezii (mikrolaryngoskopii) bylo hodnoceno 34,2 % (26/76) lézí jako nesuspektní; 39,5 % (30/76) jako suspektní; 26,3 % (20/76) lézí nebylo pro hyperkeratózu možné validně hodnotit. SE, SP, PPV, NPV a ACC pro NBI dosáhla 71,4 %; 100 %; 100 %; 53,8 % a 78,6 %, k indexu 0,556. V ECE bylo hodnoceno 30,3 % (23/76) lézí jako nesuspektní; 54,1 % (40/74) jako suspektní; 17,1 % (13/76) bylo nehodnotitelných. SE, SP, PPV, NPV a ACC dosáhla 86,4 %; 89,5 %; 95,0 %; 73,9 % a 87,3 %, k index 0,716 (tab. 2). Díky těsnému kontaktu se sliznicí u ECE bylo oproti samotnému NBI možné navíc zobrazit a hodnotit o 20 % (9/45) více lézí charakteru leukoplakií.
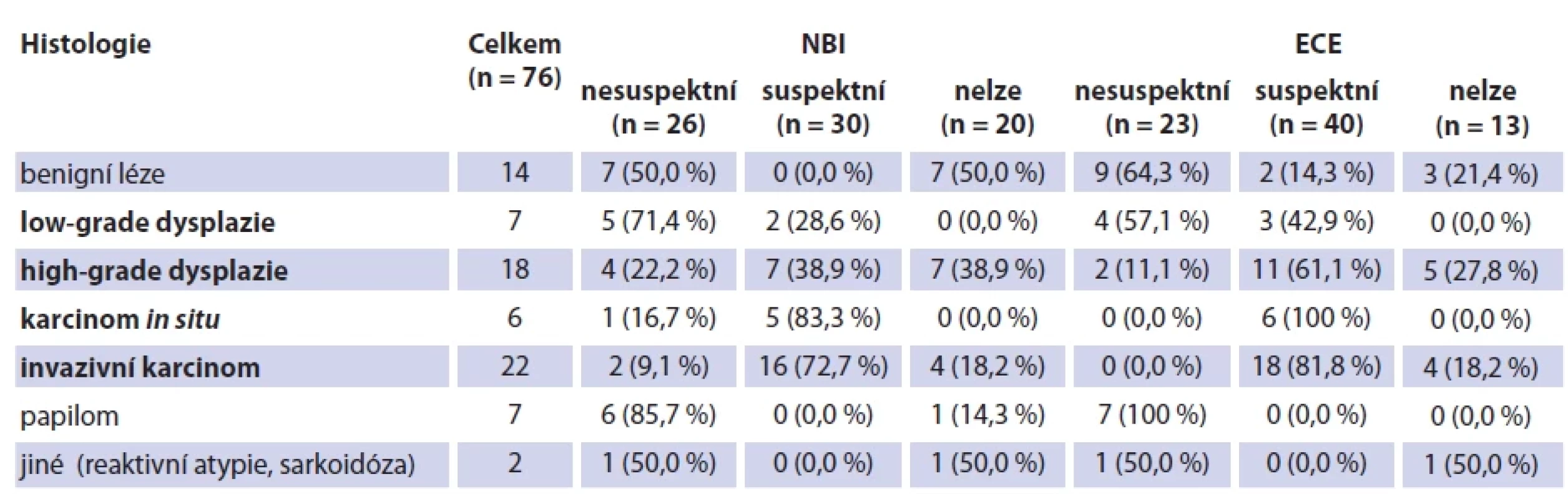
Histologické spektrum diagnóz a hodnocení v NBI a ECE ukazuje tab. 3. Benigní lézi jsme prokázali u 14 pacientů (cysta, polyp, chronická laryngitida), papilom u 7 pacientů, prekancerózu u 31 pacientů (low‑grade a high‑grade dysplazie, karcinom in situ) a invazivní karcinom u 22 pacientů.
Při hodnocení kvality jednotlivých vyšetřovacích modalit pomocí ROC analýzy jsme dosahovali vyšších hodnot AUC při použití ECE (0,879) oproti NBI (0,857) (graf 1). V grafu je dále znázorněna změna citlivosti metody v případě, kdy jsou low‑grade dysplazie zařazeny mezi benigní léze, tak jak je to u klasifikace dle Ni. Diagnostickou sílu ELS klasifikace („diagnostic performance“) na základě schopnosti odhalit prekancerózu či malignitu ukazuje graf 2.

sarkoidóza
Graph 2. Alluvial flow chart – distribution of ELS classification (perpendiclar and longitudinal vascular changes), histopathological
result and assessment of the lesion in ECE.
LGD – low-grade dysplasia, HCG – high-grade dysplasia, CIS – carcinoma in situ, SCC – invasive squamous cell carcinoma, others – reactive atypia, sarcoidosis
Diskuze
Ve srovnání s literaturou dosáhly hodnoty v našem souboru mírně horších výsledků – senzitivita, specificita, PPV, NPV a správnost ECE vyšetření byly 86,4 %; 89,5 %; 95,0 %; 73,9 % a 87,3 %. Šifrer et al. ve své publikaci při využití NBI a ELS klasifikace udávají SE, SP, PPV, NPV a ACC s hodnotami 100 %, 95 %, 88 %, 100 % a 96 % [9]. Při statistickém zpracování výsledků optických technik hraje významnou roli zvolená klasifikace a zařazení low‑grade dysplazie. V případě ELS klasifikace je na low‑grade dysplazii pohlíženo jako na suspektní lézi – přítomnost perpendikulárních vaskulárních změn, a je tak řazena mezi malignity. Naproti tomu při klasifikaci dle Ni je low‑grade dysplazie řazena ještě mezi benigní léze – stupeň IV, nesuspektní. Na tuto diskrepanci a významný podíl na výsledcích poukazují již jiní autoři [9, 12]. Při využití Ni klasifikace u jiných autorů jsou zmiňované hodnoty udávány mezi 88,9 a 97 %, 84,6 a 96 %, 90,9 a 93 %, 91,6 a 99 %, resp. 95,1 a 97 % [5, 6, 13, 14]. Pokud bychom v našem souboru pohlíželi na low‑grade dysplazie jako na benigní léze, pak by naše výsledky SE, SP, PPV, NPV a ACC dosahovaly pro NBI hodnot 80,0 %; 90,5 %; 93,3 %; 73,1 % a 83,9 %, pro ECE pak 94,6 %; 80,8 %; 91,4 %; 87,5 % a 91,3 %. V tomto případě jsou zjištěné výsledky ve shodě s literaturou.
Nižší senzitivitu si autoři vysvětlují také snahou hodnotit všechny nálezy včetně leukoplakií a hyperkeratóz oproti mnohým autorům, kteří tyto potenciálně problematické léze ze souborů vyřadili. Svou roli také může hrát tzv. křivka učení („learning curve“), na našem pracovišti byla již dlouholetá zkušenost s využitím NBI, avšak kontaktní endoskopie byla zavedena v roce 2020, postupem času tak lze očekávat dosažení vyšší schopnosti správné diferenciace slizničních lézí [15–17]. V tomto smyslu je důležité, aby se vyšetření na pracovišti provádělo pravidelně, erudovanými lékaři, školenými v hodnocení hrtanových slizničních lézí.
Mehlum et al. [3] ve své prospektivní multicentrické studii udávají SE a SP pro NBI 58 % a 76 %, horší výsledky ve srovnání s ostatními autory vysvětlují retrospektivním designem ostatních studií a srovnávání výsledků na jednom pracovišti, kdy léze posuzují 1–2 experti [5, 6, 13, 14, 18, 19]. Přínos naší studie také shledáváme v prospektivním designu, který by měl lépe odpovídat realitě, a současně lze sledovat křivku učení.
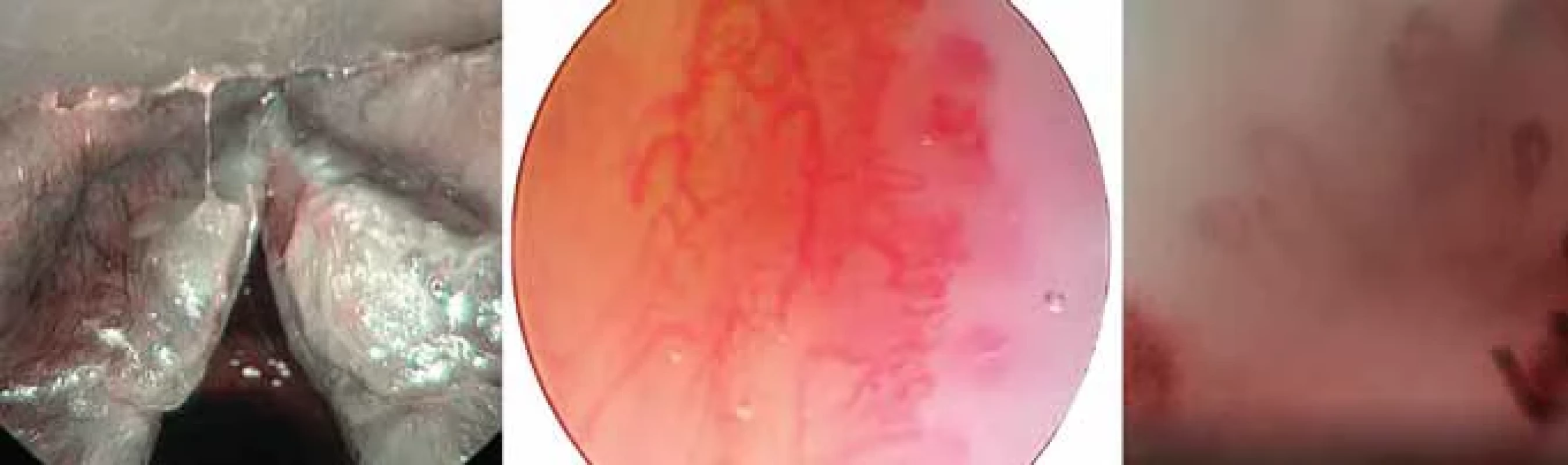
V současnosti se k hodnocení slizničních lézí v hrtanu doporučuje tzv. strukturované hodnocení léze (obr. 3a–d), tedy postupné vyšetřování různými modalitami a jejich kombinací. Výsledky potvrdily, že optimální je kombinace dvou technik (NBI + CE) než využití jedné metody [3, 7, 8, 20–22]. Zavedení ECE do běžné praxe při chirurgickém ošetření lézí hlasivek by mělo přispět k zachování onkologické bezpečnosti ve smyslu radikality a k současnému zachování kvality hlasu, cílem je vyšetřit a ošetřit lézi při jednom výkonu a zamezit opakovanému odebírání biopsií [23].
Problematickou oblastí zůstává hodnocení a přístup k leukoplakiím. Leukoplakie mají široké spektrum histologických diagnóz, jejich nebezpečí spočívá v riziku malignizace, které se udává mezi 1 a 40 % [24, 25]. Patří mezi obtížně hodnotitelné léze, kdy se často nedaří přes vrstvu hyperkeratózy validně zobrazit slizniční vaskularizaci, tzv. umbrella effect (obr. 4a–c). To se pak také promítá do horších výsledků ve srovnání s ostatními klinickými diagnózami. Hyperkeratóza a krvácení patří k limitům jak NBI, tak ECE, přesto díky těsnému kontaktu se sliznicí a výraznému zvětšení umožní ECE oproti NBI hodnotit více lézí a je přesnější. Aby nedocházelo k nadměrnému či nedostatečnému ošetření léze, je snaha rozdělit leukoplakie na low-risk a high-risk, hodnocení se provádí nejen na základě změn slizniční vaskularizace, ale také na základě celkového vzhledu, povrchu a okrajů léze [5, 6, 13, 14, 24, 25].
Mezi další metody využívané pro posuzování lézí patří hodnocení kmitání hlasivky pomocí videostroboskopie [20, 26] či videokymografie [21] nebo injektáž (hydrodisekce) hlasivky posuzující fixaci sliznice k okolí [27]. Senzitivita udávaná pro první dvě metody je poměrně dobrá: 85 % a 89 %, avšak specificita nízká: 34 % a 19 %, naopak tomu je u injektáže hlasivky: SE a SP 32 % a 87 % [3]. Lze také využít další horizontální endoskopické metody, jako je autofluorescence či vertikální optické metody [28, 29].
Bylo prokázáno, že hodnocení nálezů dle ELS klasifikace je diagnosticky efektivní z hlediska detekování maligních lézí (viz bilanční diagram, graf 2). Přítomnost perpendikulárních vaskulárních změn se prokazuje jako jeden z nejpřesnějších indikátorů malignity [3, 8, 9]. Validaci ELS klasifikace s výbornou shodou pozorovatelů mezi dvěma nezávislými pracovišti (IR – interrater reliability) k > 0,81 provedli ve své práci již Missale et al. [18]. Výborné výsledky lze vysvětlit především jednoduchým dichotomickým rozdělením lézí u ELS klasifikace, oproti tomu složitější rozdělení dle Ni dosáhlo nižších hodnot IR k = 0,55–0,69 [30, 31]. V budoucnu jistě bude implementováno počítačové zpracování a vyhodnocování nálezů pomocí umělé inteligence [32, 33], dále by také bylo vhodné zhodnotit přínos ECE pro hodnocení u pacientů po radioterapii [34, 35].
Závěr
Dle výsledků práce se potencovaná kontaktní endoskopie jeví jako přínosný nástroj pro přesnější předhistologické vyšetření slizničních lézí hrtanu. Klasifikace Evropské laryngologické společnosti je diagnosticky efektivní pro detekci maligních změn. Hlavními limity vyšetření jsou pro rigidní optiku těžce dosažitelné léze (např. dolní plocha hlasivky), krvácení a hyperkeratóza. Přesto díky těsnému kontaktu se sliznicí a výraznému zvětšení léze umožní oproti NBI hodnotit přesněji více lézí. ECE může být přínosná pro hodnocení některých leukoplakií, zvolení správného terapeutického postupu s cílem dostatečné onkologické radikality a současně se zachováním přijatelné kvality hlasu.
Prohlášení o střetu zájmů
Autor práce prohlašuje, že v souvislosti s tématem, vznikem a publikací tohoto článku není ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou. Toto prohlášení se týká i všech spoluautorů.
Grantová podpora
Podpořeno GAUK, projekt č. 506122. Tento výstup vznikl v rámci programu Cooperatio, vědní oblasti SURG. Veškerá práva podle předpisů na ochranu duševního vlastnictví jsou vyhrazena.
Zdroje
1. Dowthwaite S, Szeto C, Wehrli B et al. Contact endoscopy as a novel technique in the detection and diagnosis of oral cavity and oropharyngeal mucosal lesions in the head and neck. J Laryngol Otol 2014; 128 (2): 147–152. Doi: 10.1017/S0022215113003332.
2. Nocini R, Molteni G, Mattiuzzi C et al. Updates on larynx cancer epidemiology. Chin J Cancer Res 2020; 32 (1): 18–25. Doi: 10.21147/ j.issn.1000-9604.2020.01.03.
3. Mehlum CS, Kjaergaard T, Grontved AM et al. Value of pre- and intraoperative diagnostic methods in suspected glottic neoplasia. Eur Arch Otorhinolaryngol 2020; 277 (1): 207–215. Doi: 10.1007/s00405-019-05698-w.
4. Weller MD, Nankivell PC, McConkey C et al. The risk and interval to malignancy of patients with laryngeal dysplasia; a systematic review of case series and meta-analysis. Clin Otolaryngol 2010; 35 (5): 364–372. Doi: 10.1111/j.1749-4486.2010.02181.x.
5. Bertino G, Cacciola S, Fernandes WB et al. Effectiveness of narrow band imaging in the detection of premalignant and malignant lesions of the larynx: validation of a new endoscopic clinical classification. Head Neck 2015; 37 (2): 215–222. Doi: 10.1002/hed.23582.
6. Ni XG, He S, Xu ZG et al. Endoscopic diagnosis of laryngeal cancer and precancerous lesions by narrow band imaging. J Laryngol Otol 2011; 125 (3): 288–296. Doi: 10.1017/S0022215 110002033.
7. Puxeddu R, Sionis S, Gerosa C et al. Enhanced contact endoscopy for the detection of neoangiogenesis in tumors of the larynx and hypopharynx. Laryngoscope 2015; 125 (7): 1600–1606. Doi: 10.1002/lary.25124.
8. Arens C, Piazza C, Andrea M et al. Proposal for a descriptive guideline of vascular changes in lesions of the vocal folds by the committee on endoscopic laryngeal imaging of the European Laryngological Society. Eur Arch Otorhinolaryngol 2016; 273 (5): 1207–1214. Doi: 10.1007/s00405-015-3851-y.
9. Sifrer R, Rijken JA, Leemans CR et al. Evaluation of vascular features of vocal cords proposed by the European Laryngological Society. Eur Arch Otorhinolaryngol 2018; 275 (1): 147–151. Doi: 10.1007/s00405-017-4791-5.
10. WHO Classification of Head and Neck Tumours; Organisation mondiale de la santé, Centre international de recherche sur le cancer. WHO classification of tumours; 4th ed.; International agency for research on cancer: Lyon 2017.
11. Odell E, Eckel HE, Simo R et al. European Laryngological Society position paper on laryngeal dysplasia Part I: aetiology and pathological classification. Eur Arch Otorhinolaryngol 2021; 278 (6): 1717–1722. Doi: 10.1007/s00405-020-06403-y.
12. Kantor P, Stanikova L, Svejdova A et al. Narrative Review of Classification Systems Describing Laryngeal Vascularity Using Advanced Endoscopic Imaging. J Clin Med 2022; 12 (1). Doi: 10.3390/jcm12010010.
13. Ni XG, Wang GQ. The Role of Narrow Band Imaging in Head and Neck Cancers. Curr Oncol Rep 2016; 18 (2): 10. Doi: 10.1007/s11912-015-0498-1.
14. Kraft M, Fostiropoulos K, Gurtler N et al. Value of narrow band imaging in the early diagnosis of laryngeal cancer. Head Neck 2016; 38 (1): 15–20. Doi: 10.1002/hed.23838.
15. Ni XG, Wang GQ, Hu FY et al. Clinical utility and effectiveness of a training programme in the application of a new classification of narrow- -band imaging for vocal cord leukoplakia: A multicentre study. Clin Otolaryngol 2019; 44 (5): 729–735. Doi: 10.1111/coa.13361.
16. Dias-Silva D, Pimentel-Nunes P, Magalhaes J et al. The learning curve for narrow--band imaging in the diagnosis of precancerous gastric lesions by using web-based video. Gastrointest Endosc 2014; 79 (6): 910–920; quiz 983.e911–983.e914. Doi: 10.1016/j.gie.2013.10.020.
17. Tirelli G, Piovesana M, Bonini P et al. Follow-up of oral and oropharyngeal cancer using narrow--band imaging and high-definition television with rigid endoscope to obtain an early diagnosis of second primary tumors: a prospective study. Eur Arch Otorhinolaryngol 2017; 274 (6): 2529–2536. Doi: 10.1007/s00405-017-4515-x.
18. Missale F, Taboni S, Carobbio ALC et al. Validation of the European Laryngological Society classification of glottic vascular changes as seen by narrow band imaging in the optical biopsy setting. Eur Arch Otorhinolaryngol 2021; 278 (7): 2397–2409. Doi: 10.1007/s00405-021-067 23-7.
19. Galli J, Settimi S, Mele DA et al. Role of Narrow Band Imaging Technology in the Diagnosis and Follow up of Laryngeal Lesions: Assessment of Diagnostic Accuracy and Reliability in a Large Patient Cohort. J Clin Med 2021; 10 (6). Doi: 10.3390/jcm10061224.
20. Rzepakowska A, Sobol M, Sielska-Badurek E et al. Morphology, Vibratory Function, and Vas- cular Pattern for Predicting Malignancy in Vocal Fold Leukoplakia. J Voice 2020; 34 (5): 812.e815–812.e819. Doi: 10.1016/j.jvoice.2019.04.001.
21. Patel R, Dailey S, Bless D. Comparison of high-speed digital imaging with stroboscopy for laryngeal imaging of glottal disorders. Ann Otol Rhinol Laryngol 2008; 117 (6): 413–424. Doi: 10.1177/000348940811700603.
22. Peretti G, Piazza C, Berlucchi M et al. Pre- and intraoperative assessment of mid-cord erythroleukoplakias: a prospective study on 52 patients. Eur Arch Otorhinolaryngol 2003; 260 (10): 525–528. Doi: 10.1007/s00405-003-05 84-0.
23. Remacle M, Van Haverbeke C, Eckel H et al. Proposal for revision of the European Laryngological Society classification of endoscopic cordectomies. Eur Arch Otorhinolaryngol 2007; 264 (5): 499–504. Doi: 10.1007/s00405-007-02 79-z.
24. Pietruszewska W, Morawska J, Rosiak O et al. Vocal Fold Leukoplakia: Which of the Classifications of White Light and Narrow Band Imaging Most Accurately Predicts Laryngeal Cancer Transformation? Proposition for a Diagnostic Algorithm. Cancers (Basel) 2021; 13 (13). Doi: 10.3390/cancers13133273.
25. Li C, Zhang N, Wang S et al. A new classification of vocal fold leukoplakia by morphological appearance guiding the treatment. Acta Otolaryngol 2018; 138 (6): 584–589. Doi: 10.1080/00016489.2018.1425000.
26. van Balkum M, Buijs B, Donselaar EJ et al. Systematic review of the diagnostic value of laryngeal stroboscopy in excluding early glottic carcinoma. Clin Otolaryngol 2017; 42 (1): 123–130. Doi: 10.1111/coa.12678.
27. Zeitels SM. Premalignant epithelium and microinvasive cancer of the vocal fold: the evolution of phonomicrosurgical management. Laryngoscope 1995; 105 (3 Pt 2): 1–51. Doi: 10.1288/00005537-199503001-00001.
28. Arens C, Malzahn K, Dias O et al. Endoscopic imaging techniques in the diagnosis of laryngeal carcinoma and its precursor lesions. Laryngorhinootologie 1999; 78 (12): 685–691. Doi: 10.1055/s-1999-8775.
29. Lukeš P, Lukešová E, Zábrodský M et al. Endoskopické optické zobrazovací metody v diagnostice nádorů hrtanu. Cas Lek Cesk 2017; 156: 192–196.
30. Nogues-Sabate A, Aviles-Jurado FX, Ruiz-Sevilla L et al. Intra and interobserver agreement of narrow band imaging for the detection of head and neck tumors. Eur Arch Otorhinolaryngol 2018; 275 (9): 2349–2354. Doi: 10.1007/s0 0405-018-5063-8.
31. Zwakenberg MA, Dikkers FG, Wedman J et al. Narrow band imaging improves observer reliability in evaluation of upper aerodigestive tract lesions. Laryngoscope 2016; 126 (10): 2276–2281. Doi: 10.1002/lary.26008.
32. Esmaeili N, Illanes A, Boese A et al. Laryngeal Lesion Classification Based on Vascular Patterns in Contact Endoscopy and Narrow Band Imaging: Manual Versus Automatic Approach. Sensors (Basel) 2020; 20 (14). Doi: 10.3390/s20144018.
33. Esmaeili N, Illanes A, Boese A et al. Novel automated vessel pattern characterization of larynx contact endoscopic video images. Int J Comput Assist Radiol Surg 2019; 14 (10): 1751–1761. Doi: 10.1007/s11548-019-02034-9.
34. Šatanková J, Švejdová A, Vošmik M et al. Význam flexibilní endoskopie s Narrow Band Imaging pro hodnocení recidivy nádorů hrtanu a hypofaryngu po radioterapii. Otorinolaryngol Foniatr 2021; 70 (4): 214–222. Doi: 10.48095/ccorl2021214.
35. Zabrodsky M, Lukes P, Lukesova E et al. The role of narrow band imaging in the detection of recurrent laryngeal and hypopharyngeal cancer after curative radiotherapy. Biomed Res Int 2014; 2014: 175398. Doi: 10.1155/2014/175398.
ORCID autorů
Přijato k recenzi: 29. 5. 2023
Přijato k tisku: 25. 7. 2023
MUDr. Anna Švejdová
Klinika otorinolaryngologie a chirurgie hlavy a krku
LF UK a FN Hradec Králové
Sokolská 581
500 05 Hradec Králové
anna.svejdova@fnhk.cz
Štítky
Audiologie a foniatrie Dětská otorinolaryngologie OtorinolaryngologieČlánek vyšel v časopise
Otorinolaryngologie a foniatrie
2024 Číslo 1
Nejčtenější v tomto čísle
- Přínos tenkojehlové aspirační biopsie a klasifikace Bethesda v diagnostice tumorů štítné žlázy – retrospektivní studie
- PFAPA syndróm u detí, naša skúsenosť s chirurgickou liečbou – prehľadový článok s kazuistikou
- Netuberkulózní mykobakteriální infekce v dětském věku
- Kavernózní hemangiom temporálního svalu – kazuistika
