Moderní terapeutické možnosti syndromu Freyové – analýza pěti případů
Modern therapeutic options for Frey syndrome – analysis of five cases
Introduction: Frey‘s syndrome (SF), auriculotemporal syndrome, is an often neglected complication occurring in 6–96% of patients after parotid gland surgery according to recent studies. It arises on the basis of aberrant ingrowth of parasympathetic fi bers into the sheaths of denervated sweat glands after auriculotemporal nerve damage. The syndrome is characterized by a triad of symptoms: sweating, redness and burning or even pain in connection with food intake. Diagnosing these problems is not a time-consuming process and there are a number of therapeutic options. However, the vast majority of approaches, whether surgical or non-surgical, have only a short-term effect and carry a number of complications. The application of botulinum toxin A (BTXA) represents a relatively simple, effective and safe treatment option consisting of intradermal application of the solution according to a predetermined Frey syndrome activation map. Objectives: Presentation and evaluation of pilot results of therapeutic application of BTXA in patients dia gnosed with Frey‘s syndrome. Material and methods: Retrospective analysis of a group of 5 patients who underwent parotid gland surgery of various extents at the Department of Otorhinolaryngology and Head and Neck Surgery, University Hospital at St. Anny in Brno between 2006 and 2019, in whom there was a signifi cant manifestation of SF symptoms on the basis of which BTXA was therapeutically applied. Results: Evaluating the subjective manifestations of SF in all patients in our cohort, after the application of BTXA, showed that the problems signifi cantly decreased from “annoying and reducing their quality of life” to “never” or “almost never” occurring. Objective results of the Minor test interpreted by SketchAndCalc showed a decrease in SF activation of 91.6% on average. Only two patients required re-administration of BTXA at 6 and 19 months intervals. No adverse reactions to BTXA were reported or observed with any of the patients. Conclusion: BTXA is an eff ective and safe way to treat patients with Frey‘s syndrome.
Keywords:
parotidectomy – Frey syndrome – auriculotemporal syndrome – gustatory sweating – botulinum A toxin
Autoři:
M. Hudečková 1
; E. Minks 2
; P. Urbánková 1
; B. Gál 1
Působiště autorů:
Klinika otorinolaryngologie a chirurgie hlavy a krku LF MU a FN u sv. Anny v Brně
1; I. neurologická klinika LF MU a FN u sv. Anny v Brně
2
Vyšlo v časopise:
Otorinolaryngol Foniatr, 72, 2023, No. 2, pp. 91-100.
Kategorie:
Kazuistika
doi:
https://doi.org/10.48095/ccorl202391
Souhrn
Úvod: Syndrom Freyové (SF), aurikulotemporální syndrom, je často opomíjená komplikace vyskytující podle recentních prací u 6–96 % pacientů po operaci příušní žlázy. Vzniká na podkladě aberantního prorůstání parasympatických vláken do pochev vláken denervovaných potních žlázek po přerušení aurikulotemporálního nervu. Pro syndrom je charakteristická triáda příznaků: pocení, zarudnutí a pálení až bolest v návaznosti na příjem potravy. Dia gnostika těchto potíží je časově nenáročný proces a existuje celá řada terapeutických možností. Naprostá většina, ať už chirurgických, nebo nechirurgických přístupů má však pouze krátkodobý účinek a nesou s sebou rizika řady komplikací. Aplikace botulotoxinu A (BTXA) představuje poměrně jednoduchou, účinnou a bezpečnou možnost terapie spočívající v intradermální aplikaci preparátu podle předem stanovené mapy aktivace syndromu Freyové. Cíle: Prezentace a zhodnocení pilotních výsledků terapeutické aplikace BTXA u pacientů s diagnostikovaným syndromem Freyové. Materiál a metodika: Retrospektivní analýza souboru 5 pacientů, kteří na Klinice otorinolaryngologie a chirurgie hlavy a krku Fakultní nemocnice u sv. Anny v Brně podstoupili operaci příušní žlázy různého rozsahu v rozmezí let 2006–2019, u nichž došlo k významné manifestaci symptomů SF na základě čehož u nich byl terapeuticky aplikován BTXA. Výsledky: Vyhodnocením subjektivních projevů SF u všech pacientů z našeho souboru došlo po aplikaci BTXA k signifi kantní ústupu potíží z „obtěžujících a snižujících jejich kvalitu života“ na „nikdy“ nebo „téměř nikdy“ se nevyskytující. Objektivizací Minorovým testem interpretovaným pomocí aplikace SketchAndCalc byl prokázán ústup aktivace SF průměrně o 91,6 %. Pouze u dvou pacientů bylo nutné opakovat aplikaci BTXA v odstupu 6 a 19 měsíců. U žádného z pacientů nebyly zaznamenány nežádoucí účinky aplikace BTXA. Závěr: Aplikace BTXA představuje účinný a bezpečný způsob terapie pacientů se syndromem Freyové.
Klíčová slova:
parotidektomie – botulotoxin A – syndrom Freyové – aurikulotemporální syndrom – chuťové pocení
Úvod
Syndrom Freyové (SF), v literatuře též nazýván jako syndrom gustatorického pocení či aurikulotemporální syndrom, je pojmenován po polské neuroložce Łucji Frey, která roku 1923 ve svém článku poprvé uvedla hypotézu vzniku SF tak, jak je uznávána dnes [1]. Jedná se o častou komplikaci chirurgie příušní žlázy, ale raritně se s ním setkáváme i u tupých poranění aurikulotemporální oblasti, u zlomenin čelistního kloubu i jako následek hnisavé parotitidy či diabetické neuropatie [2, 3].
Etiologie
Etiologie SF není dosud zcela objasněna. Široce přijímanou teorií, jak ji popsala Łucja Frey, je patogeneze SF na podkladě aberantního prorůstání parasympatických vláken se sekretorickou aktivitou do pochev nervů denervovaných potních žlázek po přerušení vláken aurikulotemporálního nervu, např. během operace příušní žlázy [4].
Incidence, symptomatologie
V přechodné podobě a s minimální symp tomatologií se syndrom Freyové vyskytuje prakticky u všech pacientů v odstupu 3–12 měsíců po parotidektomii. Incidence podle literárních údajů je uváděna v širokém rozmezí od 6 do 96 %, avšak v pouhých 15 % případů činí pacientům významné subjektivní potíže a zhoršuje jejich kvalitu života [2, 5–7]. Klasickou triádou příznaků je hyperhidróza postižené oblasti, zarudnutí a parestezie až bolest zejména v návaznosti na příjem potravy [4].
Dia gnostika
Dia gnostika je v běžné praxi ORL ambulance postavena na anamnéze pacienta a jeho subjektivních potížích, pro objektivizaci je prováděn Minorův test (MT). V literatuře se dále setkáváme i s možnostmi objektivizace pomocí termografie, vyšetření pomocí savého papíru (blotting paper – BP) či s metodou histogramu papíru sublimovaného jódem (the iodine sublimated paper histogram – ISPH) [8, 9]. Minorův test spočívá v aplikaci jodové tinktury na vyšetřovanou oblast, a to v rozsahu prea infra urikulárně. Po zaschnutí je v tenké vrstvě nanesen bramborový škrobový prášek a pacient je vyzván, aby 10 minut popíjel citronovou štávu. V případě pozitivního výsledku dojde k vytvoření modročerných okrsků až splývající mapy. BP je kvantitativní metoda srovnávající změnu hmotnosti před a po absorpci potu, ISPH využívá běžné archy kancelářského papíru obsahující různá množství škrobu, které jsou nasublimovány jódem – po přiložení na obličej a po aktivaci SF získají v místě aktivace modrou barvu. Výsledek je po zaschnutí naskenován a podroben algoritmu histogramu [9].
Prevence
Preventivní a terapeutické postupy vycházejí z anatomicko-patologického podkladu vzniku SF. Z preventivních postupů se již během operace ponechává dostatečně široký kožní kryt nad lůžkem operované příušní žlázy či je využito tzv. interpozičních laloků. Oba tyto postupy mají za cíl vytvořit bariéru před vznikem abnormální inervace [2, 10]. Jako interpoziční laloky jsou užívány aloplastické a alogenní štěpy, lyofi lizovaná dura mater, tukově-kožní vrstvy či je provedena transpozice vaskularizovaného fasciálního či svalově-fasciálního štěpu, např. z povrchového muskuloaponeurotického systému či z temporálního svalu [10]. Na našem pracovišti je standardně využívána technika rotačního svalového laloku z okraje m. sternocleidomastoideus (SCM) [2, 4].
Terapie
Terapie syndromu Freyové je dělena na chirurgickou a nechirurgickou. Z chirurgických výkonů je běžně uváděna pouze transmeatální tympanická neurektomie, kdy jsou chirurgicky přerušena parasympatická vlákna v tympanické větvi IX. hlavového nervu (Jakobsonova anastomóza). Tento přístup má až 80% úspěšnost [2]. Ostatní výkony jsou ve srovnání s potížemi pacientů příliš rizikové a v běžné praxi se neprovádějí. Jedná se zejména o přerušení n. auriculotemporalis a výkony na intrakraniální části n. glossopharyngeus či na ggl. oticum [2].
Mezi nechirurgickou terapii se běžně řadí místní i celkové anticholinergní přípravky (např. skopolamin či glykopyrolát) či preparáty s chloridem hlinitým. Tyto medikamentózní přístupy však přinášejí pouze dočasnou úlevu. K dalším nevýhodám patří i riziko lokální iritace kůže nebo i tachykardie při celkovém podání.
Aplikace botulotoxinu A
Velmi účinnou a progresivní medikamentózní alternativou léčby je intrakutánní aplikace botulotoxinu A (BTXA), která byla pro syndrom Freyové poprvé využita již v roce 1995 [11]. BTXA je uvolňován bakterií Clostridium botulinum, která produkuje celkově 7 typů neurotoxického BTX označovaných jako A–G, patogenní pro člověka jsou typy A, B, E, F a G [12]. V léčbě syndromu Freyové je využíváno botulotoxinu A, v terapeutických dávkách je považován za poměrně bezpečnou a účinnou léčbu. Princip BTXA spočívá v blokaci uvolnění acetylcholinu degradací specifi ckého proteinu presynaptické části nervosvalové ploténky, tzv. SNAP-25 (synaptosomálně asociovaný protein 25) [13]. Podle metaanalýzy uveřejněné v roce 2015 Xie et al. je průměrná doba trvání účinku BTXA 6 měsíců, může však být i trvalý bez nutnosti aplikaci opakovat [14].
Mezi nežádoucí účinky intrakutánní aplikace BTXA patří lokální bolest, riziko infekce a krvácení z jednotlivých vpichů, svalová slabost, ale i lokální obrna, která je však plně reverzibilní a trvá přibližně 3–4 měsíce do odeznění účinku BTXA [7].
Cíle práce
Cílem práce je zhodnotit a prezentovat soubor pacientů a pilotních výsledků léčebné aplikace botulotoxinu A.
Materiál a metodika
Kritéria zařazení do souboru
Retrospektivní analýza pacientů, kteří na Klinice otorinolaryngologie a chirurgie hlavy a krku Fakultní nemocnice u sv. Anny v Brně, podstoupili v letech 2006–2019 operaci pro patologii v oblasti příušní žlázy. Na základě cílených anamnestických údajů v rámci pooperačních a dispenzárních kontrol bylo vysloveno podezření na manifestaci syndromu Frey - ové, který byl následně ověřen pozitivním Minorovým testem. Zařazeni byli pouze pacienti popisující své potíže jako obtěžující a snižující kvalitu jejich života v rámci defi novaného dotazníku.
Soubor pacientů
Sledovaný soubor zahrnoval 5 pacientů dospělého věku, ve všech případech se jednalo o ženy ve věku 36–56 let (průměr 45 let). U všech pacientek se jednalo o výkony pro histologicky verifi kovaný pleomorfní adenom příušní žlázy. Rozsah operace byl specifi kován podle standardního klasifi kačního systému parotidektomií podle European Salivary Gland Society [15] (obr. 1). Nejméně radikálním výkonem, u něhož došlo k manifestaci SF, byla parciální superfi ciální parotidektomie. Naopak nejrozsáhlejším výkonem bylo řešení objemného tumoru hlubokého laloku příušní žlázy s propagací do parafaryngeálního prostoru řešeného kombinovaným přístupem transorálním a transcervikálně-transparotickým s preparací a šetřením ramifi kace lícního nervu. Ve 2 případech byla primární operace doplněna o plastiku interpozičním lalokem SCM (tab. 1). Doba od operace do prvních příznaků syndromu Freyové byla v rozmezí 4–159 měsíců (průměrně 40 měsíců) (tab. 2).
Fig. 1. Classifi cation of parotidectomies according by Quer et al. [15].
![Klasifi kační systém parotidektomií upraven podle Quer et al. [15]. <br>
Fig. 1. Classifi cation of parotidectomies according by Quer et al. [15].](https://www.orlaf.cz/media/cache/resolve/media_object_image_small/media/image_pdf/fe43b79a7e04112c7bca18ef7693e211.png)
Tab. 1. Basic characteristics of included patients.
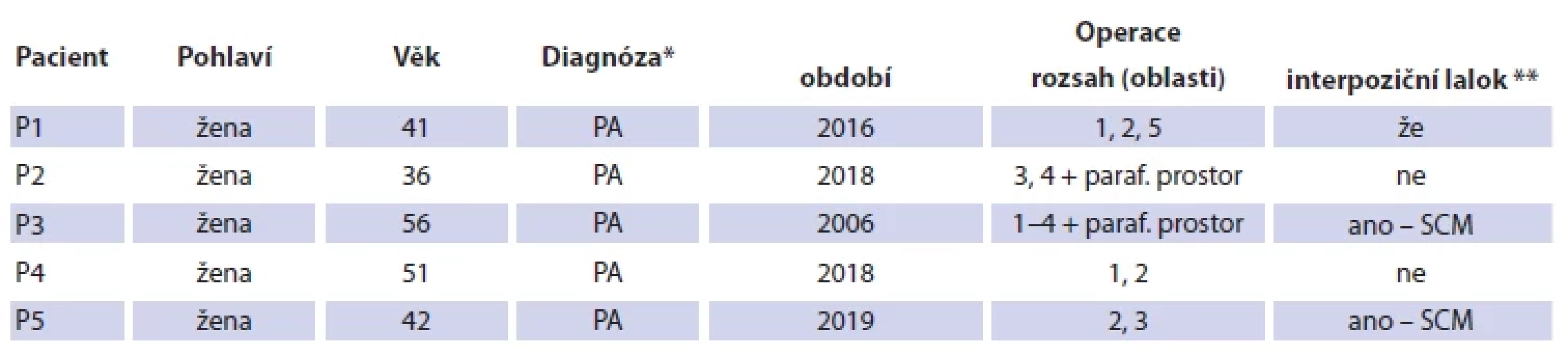
** SCM – musculus sternocleidomastoideus
Tab. 2. Symptoms of Frey‘s syndrome in a group of patients.
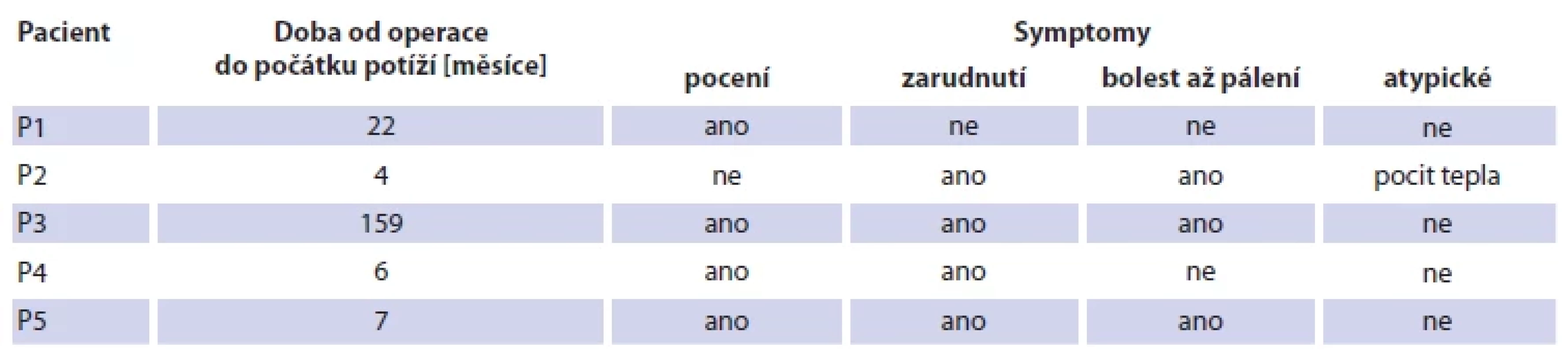
Vstupní vyšetření
Během vstupního vyšetření byli pacientky vyzvány, aby popsaly své subjektivní potíže odpovědí na dotaz, zda za poslední 2 týdny zaznamenaly v návaznosti na jídlo pocení, zarudnutí či bolesti v oblasti příušní žlázy. Svou odpověď vybíraly z 5 předem daných možností v defi novaném dotazníku (tab. 3). Do souboru pacientů byly zařazeny pacientky s odpovědí 3, 4 a 5.
Tab. 3. Entry questionnaire characterizing subjective diffi culties associated
with SF.

K objektivizaci aktivace SF bylo vy užito Minorova testu, který spočívá v potření preaurikulární a infraaurikulární oblasti jodovou tinkturou a po jejím zaschnutí je oblast pokryta jemnou vrstvou bramborového škrobu. Následně je pacient vyzván k desetiminutovému popíjení citronové šťávy. Pole aktivace SF se při pozitivním výsledku zbarví do modročerna, značící reakci potu s jodovou tinkturou a škrobem.
Výsledky MT byly vyfotografovány a interpretovány pomocí aplikace SketchAndCalc, kdy byl určen rozsah aktivace SF.
Aplikace botulotoxinu A
U pacientek bylo pro potlačení syndromu Freyové využito BTXA typu Dysport (Ipsen Pharma, Francie). Jedna ampule suchého prášku obsahuje 500 jednotek toxinu (U). BTXA byl aplikován přísně intradermálně podle předem stanovené mapy, kdy jednotlivá místa aplikace byla od sebe vzdálena zhruba 1,5 cm (obr. 2). Tímto postupem bylo u každé pacientky použito 60–120 U BTXA, průměrně 104 U. U každé členky souboru jsme zaznamenávali i komplikace spojené s aplikací BTXA – bolest při aplikaci, nežádoucí účinky bezprostředně po ošetření (tzn. v rámci 20 min po aplikaci) a pozdní komplikace.
Fig. 2. BTXA application network.

Kontrolní vyšetření
V rámci kontrolního vyšetření, které bylo plánováno na dobu po 2–4 měsících po primární aplikaci BTXA, byly pacientky opětovně vyzvány, aby své subjektivní potíže charakterizovaly podle původní škály potíží číslem 0–5 (tab. 3). Během stejné kontroly byl proveden kontrolní MT k objektivizaci účinku BTXA. U pacientek, které by své potíže i po aplikaci BTXA označily jako zhoršující kvalitu života (tedy na naší škále čísly 3–5), byla v plánu brzká reaplikace BTXA. V našem souboru se ale taková pacientka nevyskytovala.
Pacientky byly po aplikaci BTXA i nadále sledovány v rámci dispenzárních kontrol, při kterých byly cíleně dotazoványna příznaky syndromu Freyové. Při znovuobnovení potíží byl zopakován MT a provedena reaplikace BTXA – k tomu došlo u 2 pacientek z našeho souboru (tab. 4).
Tab. 4. BTXA application parameters in the presented group of patients.
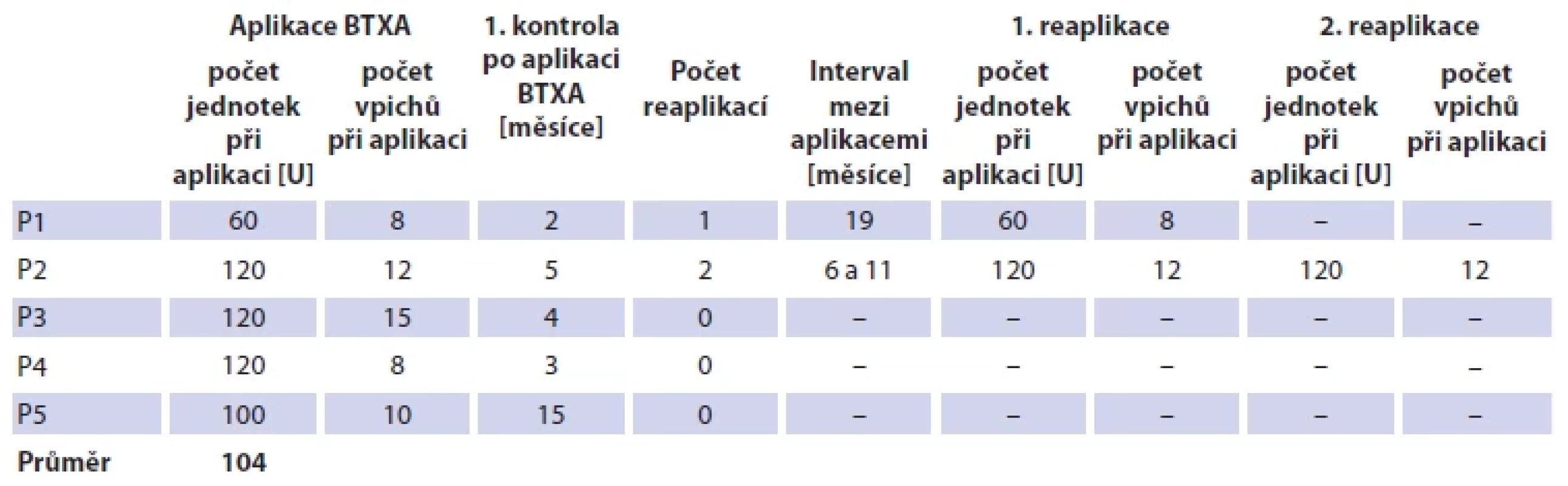

Výsledky
Podmínky zařazení do souboru splnilo celkem 5 pacientek. V rámci vstupního vyšetření byl standardně vyplněn dotazník charakterizující míru subjektivních symptomů (tab. 3). Z klasické triády příznaků bylo nejčastěji zastoupeno pocení a zarudnutí, a to vždy u 4 z 5 pacientek, bolest či pálení popsaly 3 pacientky z 5. Pouze jedna pacientka popsala atypický příznak, a to pocit tepla při konzumaci jídla. Kompletní triádu symptomů popsaly pouze 2 pacientky (tab. 2). Dvě z pěti pacientek popsaly své potíže podle použité škály hodnotou 4, což odpovídalo „častým a nepříjemným“, zbývající 3 pacientky charakterizovaly symptomy spojené se syndromem Freyové hodnotou 5 – potíže doprovázející každé jídlo a velmi zatěžující běžný život (tab. 3).
U všech 5 pacientek byl proveden MT, výsledek byl vyfotografován a následně byla plocha aktivace syndromu Freyové změřena k pozdějšímu srovnání. U všech pacientek byl MT pozitivní a plocha aktivace se pohybovala průměrně okolo 25,5 cm2 (od 11,8 cm2 do 46,6 cm2). V našem souboru plocha aktivace při Minorově testu nekorelovala se subjektivními potížemi pacientek (tab. 5). Na základě fotodokumentace byla pro každý případ vytvořena individuální mapa pro aplikaci BTXA. Během jednoho sezení bylo aplikováno průměrně 104 U BTXA (60–120 U) z 8–15 vpichů ve vzdálenostech intradermálních aplikací 1,0–1,5 cm (tab. 4). Plný účinek BTXA se u všech pacientek dostavil maximálně do 2 týdnů.
U jedné pacientky bylo potřeba aplikaci za 19 měsíců zopakovat ke korekci nově vzniklého okrsku potíží. U druhé pacientky bylo ze stejného důvodu nutno doplnit ještě 2 aplikace, a to v odstupu 6 a 11 měsíců od prvotní injektáže. U ostatních pacientek (3 z 5) bylo dosaženo dostatečného efektu již po první aplikaci BTXA (tab. 4).
Subjektivní potíže byly po aplikacích BTXA pacientkami hodnoceny v rozmezí 0–1 podle námi stanovené škály. U dvou pacientek došlo k úplnému vymizení příznaků syndromu Freyové (stupeň 0), zbylé 3 pacientky hodnotily své potíže jako téměř nikdy se nevyskytující (stupeň 1), podrobně jsou údaje uvedeny v tab. 5.
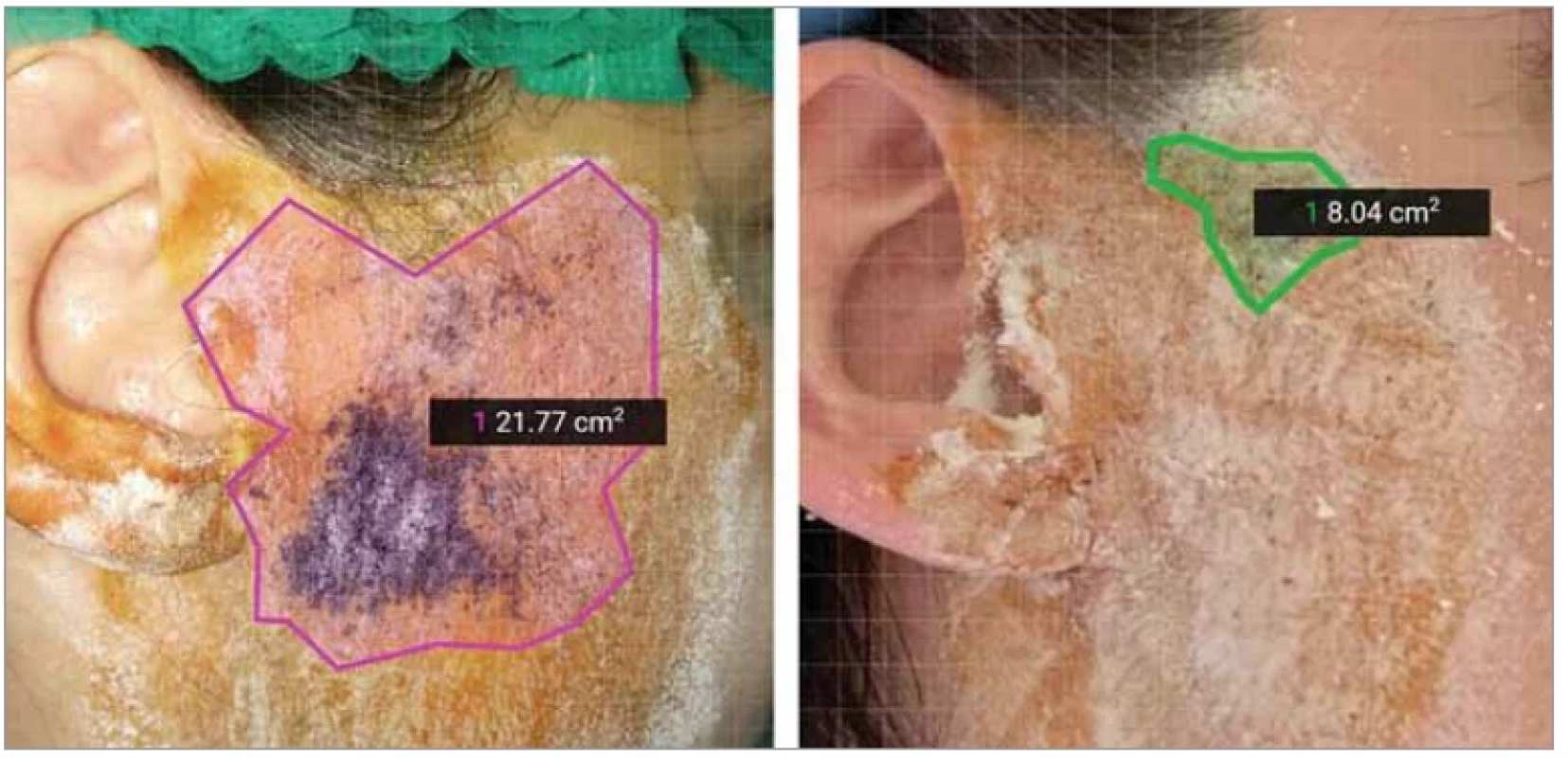
Původní plán provedení kontrolních MT byl v rozmezí 2–4 měsíce po aplikaci BTXA podle možnosti pacientek. V jednom případě ale došlo k prodloužení intervalu kontroly až na 15 měsíců z důvodu nespolupráce pacientky. Kontrolní MT byly průměrně prováděny v odstupu 6 měsíců (2–15 měsíců). Podle fotodokumentace došlo k regresi aktivace syndromu Freyové. Pozitivní plocha se po aplikaci BTXA pohybovala v průměru okolo 2,1 cm2 (0–8 cm2). Průměrné potlačení aktivace se tedy pohybovalo okolo 91,6 % (tab. 6, graf 1, obr. 3).
Tab. 6. Evaluation of the eff ect of BTXA application in a group of patients –
Minor‘s test [cm2].
![Tab. 6. Hodnocení efektu aplikace BTXA v souboru pacientů – Minorův test
[cm2]. <br>
Tab. 6. Evaluation of the eff ect of BTXA application in a group of patients –
Minor‘s test [cm2].](https://pl-master.mdcdn.cz/media/image_pdf/8854c638b989901f574a4ecd26ce6751.png?version=1684860429)
Graph 1. Evaluation of the BTXA application eff ect according to Minor’s test.

Fig. 3. Comparison of the results of Minor’s test of Patient 1. Left before BTXA application, right after BTXA application.
U žádné ze sledovaných pacientek se při aplikaci BTXA ani bezprostředně po ní neobjevily žádné nežádoucí účinky a pacientky celkově terapii aplikací BTXA hodnotily jako nebolestivou a pro ně minimálně zatěžující (podle vizuální analogové škály bolesti 0 či 1 z 10) (tab. 4).
Doba sledování pacientek v souboru byla v rozmezí 15–41 měsíců. Období dispenzarizace nekorelovala s nutností opakovat či doplňovat aplikaci BTXA.
Diskuze
Syndrom Freyové je častou komplikací chirurgie příušní žlázy vyskytující se v různé míře takřka u všech pacientů (až 96 %) v odstupu 3–12 měsíců po operaci, zánětu či úrazu v oblasti příušní žlázy. Pouze v 15 % však činí potíže trvalejšího charakteru, které pacienta limitují nebo dokonce vedou ke snížení kvality života [2, 5–7]. Podle práce Beerens a Snow z roku 2002 se ukazuje, že riziko rozvoje SF přímo koreluje s rozsahem operace. Při srovnání parciálních superfi ciálních výkonů s úplným odstraněním povrchového laloku byl výskyt SF poloviční [16]. V našem souboru pacientek bylo dia gnostikováno a aplikací BTXA léčeno 5 pacientek s manifestovanými příznaky SF. Poměrně nízkou četnost vysvětlujeme standardním postupem na našem pracovišti, kdy při významné resekci zevního laloku parotis je resekční lůžko a ramifikace lícního nervu překryta rotačním lalokem z okraje musculus sternocleidomastoideus [4].
V rámci dia gnostiky se setkáváme s mnoha úskalími. První nastává již s odhalením tohoto syndromu, často se na něj nepomýšlí a potíže spojené s bolestí v preaurikulární oblasti bývají považovány za normální pooperační stav. Navíc se cíleně na potíže se SF při kontrolách pacientů po parotidektomiích, tupých úrazech v oblasti příušní žlázy, prolongovaných hnisavých parotitidách ani při diabetické neuropatii lékař běžně neptá a pacient v naprosté většině případů o možnosti vzniku SF neví. Pokud se již vysloví podezření na SF, další úskalí spočívá v dia gnostice. Na našem pracovišti se běžně využívá MT. V práci Dulgerova et al. z roku 2000 je MT srovnáván s histogramem jódem sublimovaného papíru (ISPH), který je modifi kací MT [9]. Jako negativa MT byla uvedena špatná tolerance pacientů při aplikaci jódu na obličej a neposkytnutí trvalého záznamu výsledku [9]. Při vyšetření našich pacientů, ať už zařazených i těch do souboru nezařazených, jsme se s intolerancí lokální aplikace jódu ze strany pacientů nesetkali. Výsledky vyšetření vždy fotografujeme a snímky zařazujeme do dokumentace pacienta, aby mohly být využity při aplikaci BTXA. ISPH je technicky i časově mnohem náročnější a pro skromné využití v našich podmínkách tedy nadbytečný.
Ve snaze o definování míry subjektivních potíží pacientů bylo navrženo mnoho dotazníků [17, 18]. V rámci našeho souboru byly pokládány cílené dotazy na každý z klasické triády příznaků a následně byl cílen dotaz na potíže a případné snížení kvality života v posledních 14 dnech ve spojitosti se SF. V práci Luna Ortiz et al. z roku 2007 se setkáváme s podobně stručným dotazníkem, který cílil dotazy pouze na potíže spojené s pocením a opomíjel zarudnutí i bolest [17]. Tíže syndromu Freyové byla v této studii kromě subjektivních potíží stanovena i rozsahem aktivace SF při MT (tab. 7) [17]. V literatuře se však setkáváme i s mnohem podrobnějšími dotazníky, jako např. s dotazníkem SFIPP- -Frey scale (Sweating, Flusching, Itch, Paresthesia, Pain) uveřejněném v článku Marchese et al. v roce 2020, hodnotícím typické i atypické příznaky syndromu Freyové [18]. Kromě klasických příznaků, jako je bolest, zarudnutí a pocení, jsou pacienti vyzváni, aby se vyjádřili i ke svědění a paresteziím v operované oblasti (obr. 4).
Tab. 7. Evaluation of Frey’s syndrome severity.
According to Luna Ortiz et al. [17].
![Tab. 7. Hodnocení tíže syndromu Freyové. Upraveno podle
Luna Ortiz et al. [17]. <br>
Tab. 7. Evaluation of Frey’s syndrome severity. <br>
According to Luna Ortiz et al. [17].](https://pl-master.mdcdn.cz/media/image_pdf/e10ee673e99847eb01f4231a82f3dce8.png?version=1684860454)
Fig. 4. SFIPP – Frey scale. According to Marchese et al. [18].
![SFIPP – Frey scale. Upraveno podle Marchese et al. [18]. <br>
Fig. 4. SFIPP – Frey scale. According to Marchese et al. [18].](https://www.orlaf.cz/media/cache/resolve/media_object_image_small/media/image_pdf/06ee0677c1e3c6cb6fc95254259c1c01.png)
Léčba SF pomocí aplikace BTXA je všeobecně uznávána jako bezpečná a účinná. Náš soubor tvoří pouze 5 pacientek. Nejedná se tak o reprezentativní vzorek, ze všech případů však pouze u 2 byla zaznamenána lokální bolest při aplikaci BTXA, která brzy po ukončení ošetření odezněla. Žádný další nežádoucí účinek jsme nepozorovali. Metaanalýza Xie et al. z roku 2015 srovnávala výsledky terapie SF ve 23 studiích s celkem 411 pacienty. Z hlediska nežádoucích účinků byla nejčastěji popsána bolestivost v místě vpichů BTXA, a to v 27 případech, dále mikrohematomy z vpichů u 12 pacientů, diskrétní slabost mimických svalů u 8 pacientů, která se plně upravila v rozmezí 4–12 měsíců a u 5 pacientů se vyskytla suchost v ústech, která byla také reverzibilní nejdéle do 2 týdnů [14].
Další neopomenutelná výhoda BTXA je její účinnost. V metaanalýze Xie et al. byla popsána doba účinku průměrně 6 měsíců (3–20 měsíců) [14]. V našem souboru pacientů byl průměrný efekt BTXA dokonce 15,8 měsíce (6–20 měsíců). Tato diskrepance výsledků je však pravděpodobně dána velmi malým souborem pacientů i rozličnou dobou sledování jednotlivých případů. S účinností BTXA je spojena i potřeba její reaplikace v případech, kdy jsou potíže pacienta nezvladatelné a MT prokáže reaktivaci SF. V ně kte rých případech je BTXA aplikován i při negativním MT při výrazném zarudnutí periaurikulární oblasti v návaznosti na chuťový stimul. Tito pacienti však do našeho souboru zahrnuti nebyli.
Ohledně samotné aplikace BTXA nejsou do dnešního dne jasně stanoveny normy. V našem souboru byl BTXA aplikován ve vzdálenosti zhruba 15 mm s 10 U Dysportu na jednu intradermální aplikaci. Pro stanovení pravidel aplikace jsme vycházeli z práce Xie et al., kdy byla nejčastější vzdálenost vpichů 10 mm (průměrně 13,6 mm, rozptyl 10–20 mm) s užitím roztoku o koncentraci 2,5 U botoxu na jednu aplikaci, což odpovídá 10 U Dysportu [14]. Na problematiku správné koncentrace BTXA se ve své práci zaměřil Guntinas-Lichius, který porovnával dva soubory pacientů, u kterých použil odlišnou koncentraci BTXA při jednotlivé aplikaci, vzdálenost byla vždy 10 mm [19]. V první skupině bylo aplikováno 10 U Dysportu, ve druhé skupině 20 U Dysportu při jednom vpichu. Celkově bylo v první skupině podáno 148 ± 37 U Dysportu, ve druhé skupině 251 ± 86 U Dysportu. Podle jeho výsledků je koncentrace roztoku přímo úměrná trvání efektu BTXA – u první skupiny trval efekt 8,3 měsíce ± 2 měsíce, u druhé skupiny 16,5 měsíce ± 6 měsíců. My jsme podobného trvání efektu BTXA dosáhli již při nižší koncentraci 10 U. Otázkou však je, jakých výsledků bychom dosáhli při větším souboru pacientů nebo při zvolení vyšší koncentrace na jednu aplikaci. Podle doporučení výrobce přípravku Dysport je navíc maximální dávka pro unilaterální podání v oblasti obličeje 120 U, kterou jsme u našich pacientek nikdy nepřesáhli [20]. V souboru pacientů Guntinas-Lichius však k přesáhnutí došlo u obou skupin pacientů, i přesto však autoři ve své práci popisují absenci nežádoucích účinků u všech pacientů [19].
Efektivnost aplikace BTXA je kromě doby trvání účinku hodnocena i plochou deaktivace SF. Z mnoha analyzačních metod je nejčastěji využíván Minorův test. Naše efektivita dosáhla průměrně 91,6 % (vstupní MT průměrně 25,5 cm2, po aplikaci BTXA 2,1 cm2). Ve srovnání s prací Naumanna et al., kteří srovnávali efekt u 45 pacientů s účinností 92,6 %, jsme dosáhli takřka stejných výsledků [21]. Co se týče potlačení subjektivních potíží, jsou naše výsledky nesrovnatelné. V našem souboru u 5 pacientek došlo k takřka úplnému odstranění potíží, nesnižujících kvalitu jejich života. U poloviny sledovaného souboru Naumanna et al. došlo k úplnému potlačení potíží a zbylá polovina hodnotila své potíže jako výrazně zlepšené – vliv SF na kvalitu života nebyl v práci sledován.
Dispenzarizace pacientů byla původně plánována na 2–4 měsíce po aplikaci BTXA, avšak vzhledem k současné pandemii covidu-19 jsme volili bezkontaktní dispenzarizaci stran potíží SF formou pravidelné telefonní či e-mailové konzultace. Kontroly lokálního nálezu a zhodnocení subjektivních potíží, případně indikace k provedení MT, byly prováděny v rámci kontrol pro základní onemocnění pacienta.
Závěr
Projevy syndromu Freyové se v různé míře vyskytují téměř u všech pacientů po operaci příušní žlázy, ve vysokém procentu případů však není dia gnostikován a v návaznosti na to není pacientovi nabídnuta odpovídající terapie. V souboru našich pacientek jsme prokázali efekt aplikace BTXA na míru subjektivních potíží pacientů i na aktivaci syndromu Freyové podle Minorova testu. Podle dostupné literatury i našich zkušeností je aplikace BTXA účinnou metodou léčby syndromu Freyové u manifestovaných forem se zanedbatelnými nežádoucími účinky.
Prohlášení o střetu zájmu
Autorka práce prohlašuje, že v souvislosti s tématem, vznikem a publikací této práce není ve střetu zájmů a vznik ani publikace nebyly podpořeny žádnou farmaceutickou fi rmou.
ORCID autorů
M. Hudečková ORCID 0000-0001-8992-2033,
E. Minks ORCID 0000-0002-0037-485X,
P. Urbánková ORCID 0000-0003-2878-7661,
B. Gál ORCID 0000-0003-3351-4449.
Přijato k recenzi: 23. 5. 2022
Přijato k tisku: 3. 8. 2022
MU Dr. Markéta Hudečková
Klinika otorinolaryngologie a chirurgie
hlavy a krku
LF MU a FN u sv. Anny v Brně
Otorinolaryngol Foniatr 2023; 72(2): 91– 100
Pekařská 53
656 91 Brno
marketa.hudeckova@fnusa.cz
Zdroje
1. Frey L. Le syndrome du nerf auriculo-temporal. Rev Neurol 1923; 30: 97–104.
2. Stárek I. Pooperační komplikace chirurgické léčby slinných žláz. In: Stárek I, Černý L, Simpson RW (eds). Choroby slinných žláz. 1. vyd. Praha: Grada Publishing 2000: 253–256.
3. Bremerich A, Eufi nger H, Rustemeyer J et al. Frey Syndrom. Mund-, Kiefer- und Gesichtschirgie 2001; 5(1): 33–36. Doi:10.1007/ s100060000251.
4. Gál B, Kadaňka Z, Hložková T et al. Syndrom Freyové (aurikulotemporální syndrom) po parotidektomii a jeho prevence. Cesk Slov Neurol N 2015; 78(4): 463–467.
5. Singleton GT, Cassisi NJ. Frey‘s syndrome: incidence related to skin fl ap thickness in parotidectomy. Laryngoscope 1980; 90(10 Pt 1): 1636–1639.
6. Kornblut AD, Westphal P, Miehlke A. The eff ectiveness of a sternomastoid muscle fl ap in preventing post-parotidectomy occurrence of the Frey syndrome. Acta Otolaryngol 1974; 77(5): 368–373. Doi: 10.3109/ 00016487409124638.
7. Drobik C, Laskawi R. Frey‘s syndrome: treatment with botulinum toxin. Acta Otolaryngol 1995; 115(3): 459–461. Doi: 10.3109/ 00016489 509139348.
8. Green RJ, Endersby S, Allen J et al. Role of medical thermography in treatment of Frey‘s syndrome with botulinum toxin A. Br J Oral Maxil lofac Surg 2014; 52(1): 90–92. Doi: 10.1016/ j.bjoms.2013.09.013.
9. Dulguerov P, Quinodoz D, Cosendai G et al. Frey syndrome treatment with botulinum toxin. Otolaryngol Head Neck Surg 2000; 122(6): 821–827. Doi: 10.1016/ s0194-5998(00)70008-8.
10. Eckardt A, Kuettner C. Treatment of gustatory sweating (Frey‘s syndrome) with botulinum toxin A. Head Neck 2003; 25(8): 624–628. Doi: 10.1002/ hed.10262.
11. Schulze-Bonhage A, Schroder M. Ferbert A. Botulinum toxin in the therapy of gustatory sweating. J Neurol 1996; 243: 143–146. Doi: 10.1007/ bf02444005.
12. Závodová M. Neurotoxické klostridie. In: Bednář M, Souček A, Fraňková V et al. Lékařská mikrobio logie: Bakteriologie, virologie, parazitologie. 1. vyd. Praha: Marvil 1999: 234–235.
13. Kulíková Z. Botulotoxin a jeho využití v dermatologii. Dermatol praxi 2009; 3(3): 136–138.
14. Xie S, Wang K, Xu T et al. Effi cacy and safety of botulinum toxin type A for treatment of Frey‘s syndrome: evidence from 22 published articles. Cancer Med 2015; 4(11): 1639–1650. Doi:10.1002/ cam4.504.
15. Quer M, Guntinas-Lichius O, Marchal F et al. Classifi cation of parotidectomies: a proposal of the European Salivary Gland Society. Eur Arch Otorhinolaryngol 2016; 273(10): 3307–3312. Doi: 10.1007/ s00405-016-3916-6.
16. Beerens AJ, Snow GB. Botulinum toxin A in the treatment of patients with Frey syndrome. Br J Surg 2002; 89(1): 116–119. Doi: 10. 1046/ j.0007-1323.2001.01982.x.
17. Luna Ortiz K, Rascon Ortiz M, Sanson Riofrio JA et al. Control of Frey‘s syndrome in patients treated with botulinum toxin type A. Med Oral Patol Oral Cir Bucal 2007; 12(1): E79–84.
18. Marchese MR, Bussu F, Settimi S et al. Not only gustatory sweating and flushing: Signs and symptoms associated to the Frey syndrome and the role of botulinum toxin A therapy. Head Neck 2021; 43(3): 949–955. Doi: 10.1002/ hed.26 561.
19. Guntinas-Lichius O. Increased botulinum toxin type A dosage is more eff ective in patients with Frey‘s syndrome. Laryngoscope 2002; 112(4): 746––749. Doi:10.1097/ 00005537-200 204000-00 027.
20. Státní ústav pro kontrolu léčiv. 2020 [online]. Souhrn údajů o přípravku Dysport. Dostupné z: https:/ / www.sukl.cz/ modules/ medication/ download.php?fi le= SPC167577.pdf&type=spc &as=dysport-spc
21. Naumann M, Zellner M, Toyka KV et al. Treatment of gustatory sweating with botulinum toxin. Ann Neurol 1997; 42(6): 973–975. Doi: 10.1002/ ana.410420619.
Štítky
Audiologie a foniatrie Dětská otorinolaryngologie OtorinolaryngologieČlánek vyšel v časopise
Otorinolaryngologie a foniatrie

2023 Číslo 2
Nejčtenější v tomto čísle
- Kochleární implantace jako řešení jednostranné hluchoty u dětí – první zkušenosti
- Zkušenosti s objektivním vyšetřením schopnosti polykání pomocí flexibilní endoskopie v letech 2014–2021
- Hypakuze u pacientů s Fabryho chorobou
- Porovnanie vzájomných asociácií a senzitivity jednotlivých diagnostických metód v procese identifikácie extraezofageálneho refluxu
